Expert medical al articolului
Noile publicații
Aspecte genetice și metabolice ale patogenezei osteoartritei
Ultima examinare: 08.07.2025

Tot conținutul iLive este revizuit din punct de vedere medical sau verificat pentru a vă asigura cât mai multă precizie de fapt.
Avem linii directoare de aprovizionare stricte și legătura numai cu site-uri cu reputație media, instituții de cercetare academică și, ori de câte ori este posibil, studii medicale revizuite de experți. Rețineți că numerele din paranteze ([1], [2], etc.) sunt link-uri clickabile la aceste studii.
Dacă considerați că oricare dintre conținuturile noastre este inexactă, depășită sau îndoielnică, selectați-o și apăsați pe Ctrl + Enter.
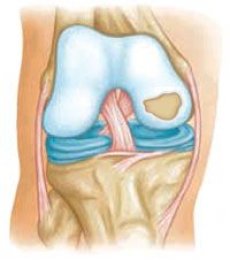
Rolul factorilor mecanici în patogeneza osteoartritei este incontestabil, dar există dovezi convingătoare că unele forme de osteoartrită sunt moștenite conform legilor lui Mendel. Osteoartropatiile ereditare pot fi împărțite în:
- osteoartrita generalizată primară (PGAO),
- artropatii asociate cu cristale,
- osteoartrita prematură cauzată de osteocondrodisplazia ereditară.
În 1803, W. Heberden a descris „ganglioni ușor denși, de mărimea unui bob de mazăre” pe suprafața dorsală a articulațiilor interfalangiene distale ale mâinilor. Acest simptom, conform autorului, distinge osteoartrita de alte boli articulare, inclusiv guta. J. Hayagarth (1805) a extins descrierea clinică a ganglionilor Heberden, menționând asocierea lor frecventă cu artroza altor localizări. Ulterior, Bouchard a descris ganglioni similari pe suprafața dorsală a articulațiilor interfalangiene proximale ale mâinilor. Folosind termenul „ganglioni Heberden și Bouchard”, W. Osier a distins „artrita hipertrofică” și „artrita deformantă” (1909). În 1953, RM Stecher și H. Hersh au descoperit prevalența ganglionilor Heberden în rândul membrilor familiei și au concluzionat că aceștia sunt moșteniți într-o manieră autosomal dominantă. Studiile ulterioare descoperirii de către RM Stecher și H. Hersh au relevat o asociere a ganglionilor Heberden și Bouchard cu leziuni degenerative ale altor articulații. Pe baza datelor examinației clinice și a tipizării HLA, JS Lawrence (1977), JS Lawrence și colab. (1983) au sugerat prezența moștenirii poligenice mai degrabă decât un defect genetic singular.
Spectrul fenotipic al osteoartritei ereditare variază foarte mult, de la forme ușoare care devin evidente clinic abia la sfârșitul vârstei adulte, până la forme foarte severe care se manifestă în copilărie. În mod tradițional, toate aceste forme au fost clasificate drept osteoartrite secundare. Acum se știe că unele dintre aceste fenotipuri sunt cauzate de mutații ale genelor care codifică macromoleculele ECM-ului cartilajului articular, care perturbă integritatea matricei cartilajului și reglarea proliferării condrocitelor și a expresiei genelor. Aceste boli ereditare reprezintă un subgrup distinct de osteoartrite, distinct de osteoartrita secundară.
Diferențe între osteoartrita ereditară și cea secundară (conform lui Williams CJ și Jimenez SA, 1999)
Osteoartrita ereditară |
Osteoartrita secundară |
|
Etiologie |
Mutația genelor exprimate în cartilajul articular |
Diverse boli ereditare și dobândite |
Patogeneză |
Leziuni ale componentelor structurale sau funcționale ale cartilajului articular |
Manifestări secundare ale bolii, care nu afectează întotdeauna doar cartilajul articular |
Tratament |
Terapia genică ar putea fi posibilă pentru a corecta defectul genetic |
Tratamentul bolii de bază |
Condrodisplazia/osteocondrodisplazia este un grup de boli clinic eterogene, caracterizate prin anomalii în creșterea și dezvoltarea cartilajului articular și a plăcii de creștere. Unele BC/OCD duc la dezvoltarea precoce a osteoartritei, caracterizată clinic printr-o evoluție severă. Printre acestea, se pot distinge următoarele boli:
- displazie spondiloepifizară (SED),
- Sindromul Stickler,
- displazie Knista,
- displazie epifizară multiplă (MED),
- condrodisplazia metafizară (MCD),
- unele displazii oto-spondilo-meta-epifizare (OSMED).
Displazii ereditare caracterizate prin osteoartrita cu debut precoce (conform Williams CJ și Jimenez SA, 1999)
Boală |
Locus |
Tipul de moștenire |
Genă mutată |
Tipul de mutație |
OA precoce cu SED cu debut tardiv (OAR)* |
12q13.1-q13.2 |
IAD |
COL 2 A, |
Substituție, inserție, ștergere de baze |
Sindromul Stickler (STL1) |
12q13.1-q13.2 |
IAD |
COL2A1 |
Înlocuirea bazei, inserarea |
Sindromul Stickler (STL2) |
6р21.3 |
IAD |
COLA |
Inserare, ștergere |
Sindromul Stickler |
1p21 |
IAD |
COLA |
Înlocuirea bazei |
Sindromul Wagner |
12q13.1-q13.2 |
IAD |
COUA, |
Înlocuirea bazei |
OSMED |
6р21.3 |
RA |
COLA |
Înlocuirea bazei |
Sindromul Marshall |
1p21 |
IAD |
COLA |
Introduce |
Displazie Knista |
12q13.1-q13.2 |
IAD |
COLA |
Inserare, ștergere |
M3fl(EDM1) |
19р13.1 |
IAD |
COMP |
Înlocuirea bazei |
MED (EDM 2) |
1р32.2-рЗЗ |
IAD |
COLA |
Introduce |
MCDS |
6q21-q22.3 |
IAD |
COLA |
Substituție de bază, ștergere |
MCDJ Jansen |
Zr21.2-pr21.3 |
IAD |
PTHR, |
Înlocuirea bazei |
*Simbolurile locusului sunt date între paranteze; AD - autosomal dominant; AR - autosomal recesiv.
Displazie spondiloepifizară
Displaziile spondiloepifizare (SED) includ un grup eterogen de boli cu transmitere autosomal dominantă, caracterizate prin dezvoltarea anormală a scheletului axial și modificări severe ale epifizelor oaselor tubulare lungi, provocând adesea nanism. SED are adesea o evoluție clinică severă, însoțită de scurtarea corpului și, într-o măsură mai mică, a membrelor.
În formele de SED care se manifestă la o vârstă mai înaintată, fenotipul este adesea puțin modificat și se poate manifesta clinic abia la adolescență, când se dezvoltă osteoartroza severă. Deformarea coloanei lombare se poate manifesta prin îngustarea discurilor intervertebrale, platispondilie și cifoscolioză minoră. De asemenea, se detectează anomalii ale epifizelor din articulațiile periferice și modificări degenerative precoce ale acestora. Cel mai constant semn al afectării articulațiilor periferice este aplatizarea suprafețelor articulare ale articulațiilor gleznei și genunchiului, precum și aplatizarea șanțului intercondilian al femurului. Anomaliile capului și gâtului femurului sunt adesea detectate odată cu dezvoltarea osteoartrozei articulației șoldului, manifestându-se în adolescență.
Întrucât colagenul de tip II este componenta majoră a matricii extracelulare a cartilajului hialin, s-a sugerat că gena care îl codifică, COL1A, este cauza SED. Prima descriere a unei legături genetice între fenotipul osteoartritei precoce asociate cu SED cu debut tardiv și gena procolagenului de tip II, COL 2 A, datează din 1989 și 1990. Primul raport al unei mutații COL 2 A la rude cu osteoartrite precoce asociată cu SED cu debut tardiv a implicat substituția bazei Arg519>Cys. Până în prezent, au fost identificate încă patru familii cu mutații similare. La membrii unei alte familii cu OA precoce și SED ușor, a fost găsită substituția bazei Arg75>Cys, deși fenotipul SED la membrii acestei familii nu este similar cu fenotipul familiei cu o substituție de la arginină la cisteină la poziția 519. Alte mutații COL 2 A-Gly976>Ser, Gly493>Ser au fost, de asemenea, găsite la membrii familiilor cu SED. J. Spranger și colab. (1994) au folosit termenul „colagenopatie de tip 11” pentru a descrie bolile ereditare ale țesutului cartilajului cu o mutație primară în gena COL1A a procolagenului de tip II.
Forma clasică a sindromului Stickler
A fost descrisă pentru prima dată în 1965 de GB Stickler și colegii săi, care au numit-o artro-oftalmopatie ereditară. Sindromul descris de GB Stickler a fost caracterizat prin deficiențe de vedere și boli articulare degenerative severe, care se dezvoltă de obicei în a treia sau a patra decadă de viață. Este o tulburare autosomal dominantă cu o incidență de aproximativ 1 la 10.000 de nou-născuți vii. Tabloul clinic include miopie, surditate progresivă, palatoschizis, hipoplazie a mandibulei (anomalie Pierre-Robin) și hipoplazie a epifizelor. În perioada neonatală, radiografiile pacienților cu sindrom Stickler relevă epifize mărite, în principal femurul proximal și tibia distală. În timpul creșterii, se dezvoltă displazie epifizară, care se manifestă prin osificarea neregulată a epifizelor și modificări degenerative ulterioare.
Întrucât COL 2 A este exprimat în cartilajul articular și în corpul vitros al globului ocular, apariția sindromului Stickler a fost asociată cu patologia acestei gene. Cu toate acestea, o examinare a mai multor familii cu sindrom Stickler a arătat că nu toate familiile au o boală asociată cu COL 2 A. Această formă a bolii se numește sindrom Stickler de tip I (simbol locus STL1).
Spectrul manifestărilor clinice ale sindromului Stickler variază foarte mult, iar până în prezent au fost identificate mai multe fenotipuri. Printre acestea se numără sindromul Wagner, care se caracterizează printr-o predominanță a afectării globului ocular; artroza în sindromul Wagner practic nu se dezvoltă niciodată, deși la pacienți a fost identificată o mutație a genei COL 2 A (substituție de bază Gly67>Asp). Rămâne neclar de ce o astfel de mutație COL compromite doar funcția corpului vitros și nu afectează cartilajul hialin.
O altă formă a sindromului Stickler este așa-numita variantă olandeză; aceasta este caracterizată prin toate manifestările clasice ale sindromului, cu excepția deficienței de vedere. HG Brunner și colab. (1994) au arătat că fenotipul olandez al sindromului Stickler este asociat cu o mutație în gena COL,,A2 : mutația dominantă este o deleție de 54 de perechi de baze, urmată de o deleție de exoni. M. Sirko-Osadsa și colab. (1998) au raportat o altă familie, fără legătură cu cea descrisă de autorii anteriori, cu un fenotip similar și o mutație în gena COL,,A2 ( deleție de 27 de perechi de baze), ceea ce confirmă datele lui HG Brunner și colab. (1994). Această variantă se numește sindrom Stickler de tip II (simbol locus STL1).
Recent, un al treilea locus al sindromului Stickler a fost identificat la membrii unei familii cu patologii vitroase și retiniene care sunt fenotipic semnificativ diferite de modificările observate în varianta „clasică” a sindromului. O mutație în gena COL2A| (substituție de bază Gly97>Val) a fost descoperită la membrii acestei familii. Desigur, sunt necesare noi descrieri ale cazurilor cu acest fenotip și genotip al sindromului Stickler pentru a confirma descoperirile lui AJ Richards și colab.
Legătura nozologică dintre sindromul Marshall și versiunea clasică a sindromului Stickler a fost discutată de mult timp. În prezent, sindromul Marshall este clasificat ca un fenotip separat, în principal datorită deformării mai pronunțate a scheletului facial, deși afectarea articulațiilor periferice este similară cu cea din sindromul Stickler de tip I. În sindromul Marshall, osteoartrita articulațiilor genunchiului și a coloanei lombosacrale începe după 30 de ani. Cauza sindromului este o mutație a genei de colagen de tip IX COL n A1.
 [ 1 ], [ 2 ], [ 3 ], [ 4 ], [ 5 ], [ 6 ]
[ 1 ], [ 2 ], [ 3 ], [ 4 ], [ 5 ], [ 6 ]
OSMED
Acest fenotip a fost descris într-o familie olandeză în care modificări degenerative ale articulațiilor, asemănătoare osteoartrozei, au apărut în adolescență și au afectat în principal articulațiile șoldului, genunchiului, cotului și umărului; s-au constatat, de asemenea, trăsături faciale particulare, lordoză lombară crescută, articulații interfalangiene mărite și pierderea auzului, dar nu au fost detectate anomalii vizuale (Vikkula M. și colab., 1995). Cercetătorii au descoperit o mutație în gena care codifică lanțul α2 al colagenului de tip II COL, A2.
Displazie Knista
Caracterizat prin scurtarea trunchiului și a membrelor, aplatizarea feței și a podului naral, exoftalmie și anomalii articulare severe. La pacienții cu sindrom Kniest, articulațiile, de obicei mari de la naștere, continuă să se mărească în copilărie și la începutul adolescenței. De asemenea, aceștia prezintă adesea miopie, pierderea auzului, palatoschizis și picior strâmb; majoritatea pacienților dezvoltă modificări degenerative severe devreme, în special pronunțate la nivelul articulațiilor genunchiului și șoldului. Radiografiile coloanei vertebrale relevă aplatizarea și alungirea semnificativă a corpurilor vertebrale și a platispondiliei. Oasele tubulare lungi sunt deformate ca o ganteră, iar osificarea epifizelor este lentă. În articulațiile mâinilor, epifizele sunt aplatizate, iar spațiile articulare sunt îngustate. Cartilajul articular este moale, elasticitatea sa este redusă; histologic, în acesta se găsesc chisturi mari (simptomul „brânză elvețiană”). Sindromul Kniest este cauzat de o mutație a genei procolagen de tip II COb2A1.
 [ 7 ], [ 8 ], [ 9 ], [ 10 ], [ 11 ], [ 12 ], [ 13 ], [ 14 ]
[ 7 ], [ 8 ], [ 9 ], [ 10 ], [ 11 ], [ 12 ], [ 13 ], [ 14 ]
Displazia epifizară multiplă (MED)
Un grup eterogen de boli caracterizate prin dezvoltarea anormală a plăcilor de creștere ale oaselor tubulare lungi, precum și prin osteoartroză severă precoce (manifestată în copilărie) care afectează atât articulațiile axiale, cât și cele periferice (cel mai adesea articulațiile genunchiului, șoldului, umărului și mâinii). Clinic, DEM se manifestă prin durere și rigiditate articulară, modificări ale mersului. Pacienții cu DEM prezintă, de asemenea, modificări minime ale coloanei vertebrale (diverse grade de aplatizare a corpurilor vertebrale), uneori coloana vertebrală fiind intactă. Statura mică a pacienților este, de asemenea, caracteristică, deși nanismul se dezvoltă rar. Organul vizual nu este afectat. DEM include mai multe variante, de exemplu, fenotipul Fairbanks și Ribbing.
Displaziile de tip MED sunt moștenite autosomal dominant, cu grade variabile de penetranță. Întrucât caracteristica MED este o anomalie a plăcii de creștere epifizare, s-a sugerat că aceste displazii sunt cauzate de un defect al genelor care codifică macromoleculele cartilajului plăcii de creștere. S-a dovedit că cel puțin trei loci sunt asociați cu fenotipul MED. Studiile realizate de EJ Weaver și colab. (1993), JT Hecht și colab. (1992) au exclus genele de colagen de tip II și VI, proteina centrală a proteoglicanilor și proteina conjunctivă a cartilajului din lista „vinovaților” de MED. JT Hecht și colab. (1993), R. Oehelmann și colab. (1994) a descoperit o legătură între MED, precum și sindromul de pseudoacondroplazie asociat clinic, și regiunea pericentromerică a cromozomului 19. Studiile ulterioare au identificat o mutație în gena care codifică proteina matricei oligomerice a cartilajului (OMMP) la trei pacienți cu MED (simbol locus EDM1). Întrucât toate cele trei mutații au apărut în regiunea genică care codifică domeniul de legare a calciului al OMMP, este probabil ca funcția de legare a calciului a acestei proteine să fie esențială pentru dezvoltarea normală a cartilajului plăcii de creștere.
MD Briggs și colab. (1994) au raportat o familie olandeză cu fenotip MED asociat cu o regiune a cromozomului 1 care conține una dintre genele de colagen de tip IX, COL1A1 (simbol al locusului EDM 2). În mod notabil, mutația descoperită a fost prima dovadă a unui rol al colagenului de tip IX, localizat pe suprafața fibrilelor de colagen II, în menținerea integrității cartilajului hialin. M. Deere și colab. (1995) au arătat că fenotipul Fairbanks nu a fost asociat genetic nici cu locusul EDM, nici cu locusul EDM2, confirmând heterogenitatea MED.
Condrodisplazia metafizară (MCD)
Un grup eterogen (au fost descrise peste 150 de tipuri) de boli ereditare ale cartilajului hialin, care se manifestă clinic ca osteoartroză precoce. Bolile metacromatice majore (MHD) sunt caracterizate prin modificări ale metafizelor osoase. Clinic, se manifestă prin statură mică, membre scurtate, tibie curbate și mers de tip „rață”. Pacienții cu MHD prezintă, de asemenea, semne de afectare a altor sisteme (de exemplu, sistemele imunitar și digestiv). Se observă dezorganizarea cartilajului plăcii de creștere, care se manifestă histologic ca grupuri de condrocite proliferate și hipertrofiate, înconjurate de septuri îngroșate și matrice dezorganizată, precum și prin penetrarea cartilajului necalcificat în osul subcondral.
Sindroamele Jansen, Schmid și McKusick sunt cele mai bine studiate MHD-uri. Acestea sunt similare în ceea ce privește caracteristicile anomaliilor scheletice, dar diferă în ceea ce privește severitatea (sindromul Jansen - sindromul McKusick - sindromul Schmid). Cel mai frecvent este sindromul Schmid (simbol al locusului MCDS), care se transmite autosomal dominant. Radiologic, sindromul se manifestă prin coxa vara, scurtarea și curbura oaselor tubulare, deformarea în formă de cupă a metafizelor (mai pronunțată în partea proximală decât în cea distală a femurului). Cele mai pronunțate modificări se observă la nivelul plăcilor de creștere ale oaselor tubulare lungi.
Cel puțin 17 tipuri diferite de mutații ale genei colagenului X au fost descrise la pacienții cu sindrom Schmid. Colagenul X este exprimat în condrocitele hipertrofiate ale plăcilor de creștere și poate fi implicat în procesele de osificare. Prin urmare, o mutație a genei colagenului X COb2A1 este cea mai probabilă cauză a sindromului Schmid.
Copiii cu sindrom Jansen prezintă hipercalcemie, niveluri crescute de fosfat urinar și niveluri scăzute de hormon paratiroidian (PTH) și peptide legate de PT. Anomalia acestuia din urmă este probabil responsabilă pentru dezvoltarea sindromului Jansen. În 1994, AS Karaplis și coautorii au publicat rezultatele unui studiu original. După perturbarea genei care codifică peptida legată de PT în celulele stem embrionare de șoarece, șoarecii cu o deficiență a acestei alele au murit imediat după naștere. S-a descoperit că aceștia prezintă o anomalie în dezvoltarea osoasă subcondrală, o creștere afectată a cartilajului și o proliferare scăzută a condrocitelor. În 1995, E. Schipani și coautorii au raportat o mutație heterozigotă în gena receptorului PTH la un pacient cu sindrom Jansen. Mutația a constat într-o substituție de bază Gys223>Arg, care a dus la acumularea de cAMP; Aceasta înseamnă că aminoacidul histidină din poziția 223 joacă un rol crucial în transmiterea semnalului. Ulterior, E. Schipani și colab. (1996) a raportat alți trei pacienți cu sindrom Jansen, dintre care doi aveau o mutație similară, iar al treilea avea o substituție TrA10>Ро.
Osteoartrita generalizată primară
Cea mai frecventă formă ereditară de osteoartrită este osteoartrita generalizată primară (OPG), care a fost descrisă pentru prima dată ca o nozologie separată de JH Kellgren și R. Moore în 1952. Clinic, osteoartrita generalizată primară se caracterizează prin apariția ganglionilor Bouchard și Heberden, leziuni poliarticulare. Osteoartrita generalizată primară se caracterizează prin debutul precoce al manifestării osteoartritei și progresia rapidă a acesteia. Radiologic, osteoartrita generalizată primară nu diferă de osteoartrita non-ereditară. În ciuda faptului că problema etiopatogenezei osteoartritei generalizate primare este încă dezbătută, studiile demonstrează rolul important al predispoziției ereditare în apariția și progresia osteoartritei generalizate primare.
Astfel, JH Kellgren și colab. (1963) au descoperit ganglioni Boucharay-Heberden la 36% dintre rudele de sex masculin și 49% dintre rudele de sex feminin, în timp ce în populația generală aceste cifre au fost de 17% și, respectiv, 26%. La persoanele cu osteoartrita generalizată primară, haplotipul HLA A1B8 și izoforma MZ a α1-antitripsinei sunt mai des detectate. Într-un studiu clasic care a implicat gemeni, TD Spector și colab. (1996) au efectuat radiografii ale articulațiilor genunchiului și ale articulațiilor mâinii la 130 de gemene monozigote și 120 de gemene fraterne pentru modificări caracteristice osteoartritei. S-a constatat că concordanța semnelor radiografice ale osteoartritei tuturor localizărilor a fost de 2 ori mai mare la gemenii monozigoți comparativ cu gemenii fraterni, iar contribuția factorilor genetici a variat de la 40 la 70%. Un studiu al osteoartritei nodulare realizat de GD Wright și colab. (1997) a demonstrat debutul precoce al bolii, severitatea ridicată și o corelație negativă între vârsta de debut a bolii la pacienți și vârsta de concepție a părinților acestora.
Printre artropatiile asociate cristalelor, depunerea de cristale de acid uric și cristale care conțin calciu în cavitatea articulară are o predispoziție familială.
Artropatii ereditare asociate cu cristale (conform lui Williams CJ și Jimenez SA, 1999)
Boală |
Locus |
Tipul de moștenire |
Genă mutată |
Tipul de mutație |
Gută (HPRT)* |
Xq27 |
Legat de X |
HPRT1 |
Substituție de bază, ștergere |
Gută (PRPS) |
Xq22-q24 |
Legat de X |
PRPS1 |
Înlocuirea bazei |
Artropatia primară cu pirofosfat (CCAL1) |
5р15.1-р15.2 |
IAD |
? |
? |
Artropatie pirofosfatică cu debut precoce asociată cu 0A (CCAL2) |
8q |
IAD |
? |
? |
*Simbolurile locusului sunt date între paranteze; AD – autosomal dominant.
În 1958, D. Zintann S. Sitaj a prezentat descrieri clinice ale unei patologii pe care au numit-o „condrocalcinoză” la 27 de pacienți. Majoritatea pacienților aparțineau a cinci familii, indicând o componentă ereditară în etiopatogeneza bolii. Ulterior, D. McCarty și JL Hollander (1961) au raportat cazul a doi pacienți suspectați de gută cu depunere de cristale nonurate în cavitatea articulară. Examinarea cu raze X a relevat calcificarea anormală a cartilajului hialin al multor articulații.
Radiografic, boala depunerii cristalelor de pirofosfat de calciu dihidrat, sau artropatia cu pirofosfat, seamănă cu osteoartroza sporadică, dar afectează mai des articulațiile care nu sunt tipice pentru formele comune de osteoartroză (de exemplu, articulațiile metacarpofalangiene, scaforadiale, femuro-patelo-patelare ale genunchiului). În artropatia cu pirofosfat, se formează mai des chisturi osoase subcondrale. Deși în majoritatea cazurilor, condrocalcinoza apare înainte de manifestarea osteoartrozei secundare, la unii indivizi boala poate debuta ca osteoartroză idiopatică, care este însoțită de tulburări metabolice (hemocromatoză, hiperparatiroidism, hipomagneziemie etc.).
Cel mai probabil, modificările structurale ale ECM-ului cartilajului articular induc depunerea de cristale de pirofosfat de calciu dihidrat. AO Bjelle (1972, 1981) a constatat o scădere a conținutului de colagen și fragmentarea fibrelor de colagen în zona mediană a matricei cartilajului articular la membrii familiei suedeze cu artropatie pirofosfatică. Deoarece aceste zone nu conțineau cristale, autorii au sugerat că anomalia matriceală descrisă ar putea predispune la depunerea acestora și la dezvoltarea modificărilor degenerative la nivelul articulațiilor. Pe baza unui studiu al cazurilor sporadice de artropatie pirofosfatică, K. Ishikawa și colab. (1989), I. Masuda și colab. (1991) au concluzionat că condrocalcinoza este cauzată de o mutație în genele care codifică proteinele ECM. CJ Williams și colab. (1993), AJ Reginato și colab. (1994) au descoperit o mutație heterozigotă COL 2 A (substituție de bază Argl5>Cys) la membrii unei familii numeroase cu un fenotip clinic de osteoartrită severă precoce cu anchiloză, dezvoltare tardivă a displaziei spondiloepifizare și condrocalcinoză a cartilajului hialin și fibrocartilajului. Cu toate acestea, s-a dovedit că la membrii acestei familii condrocalcinoza a fost secundară osteoartritei.
De asemenea, s-a sugerat că componentele anorganice ale ECM contribuie la formarea cristalelor. De exemplu, hipomagneziemia provoacă condrocalcinoză prin inhibarea enzimei pirofosfatază, care, la rândul ei, reduce dizolvarea cristalelor. Niveluri crescute de fosfați anorganici au fost găsite în lichidul sinovial al pacienților cu artropatie pirofosfatică. Aceasta și alte observații au sugerat că pacienții cu artropatie pirofosfatică au o tulburare locală a metabolismului pirofosfatului. A fost descrisă enzima nucleozid trifosfat pirofosfohidrolază, care poate fi implicată în formarea cristalelor de pirofosfat în zona depunerii lor în ECM. Niveluri crescute ale acestei enzime au fost găsite în cazuri sporadice de artropatie pirofosfatică, dar această anomalie nu a fost observată în formele familiale ale bolii (Ryan LM și colab., 1986). Cu toate acestea, la cultivarea fibroblastelor și limfoblastelor de la pacienți cu artropatie familială pirofosfatică, s-a detectat o creștere a conținutului de fosfați anorganici, ceea ce confirmă, de asemenea, presupunerea despre rolul tulburărilor metabolismului local al pirofosfatului în patogeneza bolii.
În ultimii ani, s-au făcut încercări de identificare a genelor „vinovate” de apariția cazurilor familiale de artropatie pirofosfatică. Astfel, analiza materialului genetic obținut de la membrii unei familii numeroase cu artropatie pirofosfatică (Maine, SUA), în care condrocalcinoza s-a dezvoltat secundar unei osteoartroze severe, cu progresie rapidă, non-displazice, a exclus o legătură între boală și locusul COL 2. Cu toate acestea, autorii acestui studiu au descoperit o legătură între fenotipul studiat al artropatiei pirofosfatice și un locus situat pe brațul lung al cromozomului 8 (simbolul locusului CCAL). A.G. Hughes și colab. (1995) au găsit o legătură între fenotipul condrocalcinozei primare într-o familie din Marea Britanie și locusul CCAL1, care este localizat pe brațul scurt al cromozomului 5 în regiunea 5p15. Conform lui C.J. Williams și colab. (1996), locusul CCAL1 la membrii unei familii argentiniene cu artropatie pirofosfatică a fost localizat ceva mai proximal decât în cazul precedent, în regiunea 5p15.1. Un genotip similar a fost găsit la membrii unei familii din Franța.
Astfel, datele din studiile descrise indică faptul că forma familială de artropatie pirofosfatică este o boală eterogenă clinic și genetic, care poate fi cauzată de mutații în cel puțin trei gene diferite.

