Expert medical al articolului
Noile publicații
Modelarea experimentală a osteoartritei la animale
Ultima examinare: 07.07.2025

Tot conținutul iLive este revizuit din punct de vedere medical sau verificat pentru a vă asigura cât mai multă precizie de fapt.
Avem linii directoare de aprovizionare stricte și legătura numai cu site-uri cu reputație media, instituții de cercetare academică și, ori de câte ori este posibil, studii medicale revizuite de experți. Rețineți că numerele din paranteze ([1], [2], etc.) sunt link-uri clickabile la aceste studii.
Dacă considerați că oricare dintre conținuturile noastre este inexactă, depășită sau îndoielnică, selectați-o și apăsați pe Ctrl + Enter.
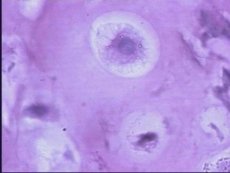
KRN Pritzker (1994) a definit un model animal experimental al oricărei boli ca fiind „un grup omogen de animale care prezintă un proces biologic moștenit, dobândit natural sau indus experimental, supus investigației științifice, care este similar într-unul sau mai multe aspecte cu boala la om”. Modelele animale de osteoartrită sunt utile pentru studierea evoluției modificărilor structurale ale țesuturilor articulare, pentru a determina modul în care diverși factori de risc inițiază sau promovează aceste modificări și pentru a evalua măsurile terapeutice. Este important să ne amintim că osteoartrita nu este o boală a unui singur țesut, cartilajul articular, ci a tuturor țesuturilor articulației afectate, inclusiv osul subcondral, membrana sinovială, meniscurile, ligamentele, mușchii periarticulari și nervii aferenți cu terminații atât în afara, cât și în interiorul capsulei articulare. Studiile agenților farmacologici la modelele animale se concentrează în principal pe efectele lor asupra cartilajului articular. Este imposibil să se evalueze principalul simptom al osteoartrozei la om - durerea articulară - în modele experimentale. În același timp, la modelarea osteoartrozei la animale, nu se iau în considerare o serie de factori importanți care contribuie la dezvoltarea și progresia osteoartrozei (de exemplu, poziția verticală a corpului uman, slăbiciunea mușchilor periarticulari etc.).
Desigur, cel mai ilustrativ model al bolii este cel care are cea mai mare asemănare cu modificările din osteoartrita umană. Modelele animale de osteoartrită prezintă cel mai mare interes în ceea ce privește studierea eficacității medicamentelor modificatoare de boală pentru osteoartrită (DMOAD). Deși o serie de medicamente din acest grup previn dezvoltarea sau încetinesc progresia osteoartritei induse experimental sau spontane la animale, toate acestea au fost ineficiente atunci când s-au studiat efectele lor la oameni.
Modele animale de osteoartrită
Mecanismul de modelare |
Specii de animale |
Factor/agent inductor |
Sursă |
Osteoartrita spontană |
Cobai |
Vârstă/supraponderalitate |
Bendele AM și colab., 1989 |
Șoareci STR/ORT, STR/INS |
Predispoziție genetică |
Das-Gupta EP și colab., 1993 Dunham J. și colab., 1989 Dunham J. și colab., 1990 |
|
Șoareci negri C57 |
Predispoziție genetică |
OkabeT., 1989 StabescyR. și colab., 1993 Takahama A.. 1990 van der Kraan PM și colab., 1990 |
|
Șoareci |
Mutația colagenului II |
Garofalo S. și colab., 1991 |
|
Șoareci |
Mutația colagenului IX |
Nakata K. și colab., 1993 |
|
Câini |
Displazie de șold |
SmaleG. și colab., 1995 |
|
Primate |
Predispoziție genetică |
Alexander CJ, 1994; Carlson CS și colab., 1994; Chateauvert JM și colab., 1990 |
|
Osteoartrita indusă chimic |
Pui |
Iodoacetat premium* |
Kalbhen DA, 1987 |
Iepuri |
Papaină premium |
Marcelon G. colab., 1976 Coulais Y. colab., 1983 Coulais Y. colab., 1984 |
|
Cobai |
Papaină premium |
Tanaka H. și colab., 1992 |
|
Câini |
Chimopapaină vs. |
Leipold HR și colab., 1989 |
|
Șoareci |
Papaină premium |
Van der Kraan PM și colab., 1989 |
|
Șoareci |
Colagenază premium |
Van der Kraan PM și colab., 1989 |
|
Șoareci |
TFR-R vs. |
Van den Berg WB. 1995 |
|
Iepuri |
Soluție hipertonică de NaCl |
VasilevV. și colab., 1992 |
|
Osteoartrita indusă fizic (chirurgical) |
Câini |
Transecția ligamentului încrucișat anterior (unilaterală) |
Marshall JL și colab., 1971; Brandt KD, 1994 |
Câini |
Transecția ligamentului încrucișat anterior (bilaterală) |
Marshall KW Chan AD, 1996 |
|
Iepuri |
Transecția ligamentului încrucișat anterior |
Christensen SB, 1983 VignonE. et al., 1991 |
|
Oaie |
Meniscectomie |
Ghosh P. și colab., 1993 |
|
Iepuri |
Meniscectomie |
FamA.G. și colab., 1995 Moskowitz RW, Goldberg VM, 1987 |
|
Cobai |
Meniscectomie |
Bendele AM, 1987 |
|
Cobai |
Miectomie |
ArseverC.L, BoleG.G., 1986 LaytonM.W. și alții, 1987 Dedrick DK și alții, 1991 |
|
Iepuri |
Contuzie patelară |
Oegema TRJ, et al., 1993 Mazieres B. et al., 1990 |
|
Iepuri |
Imobilizare |
Langenskiold A. și colab., 1979 Videman T., 1982 |
|
Câini |
Imobilizare |
Howell DS și colab., 1992; Ratcliffe A. și colab., 1994; Palmoski M., Brandt KD, 1981 |
|
Câini |
Denervare urmată de transecția ligamentului încrucișat anterior |
VilenskyJA și colab., 1994 |
* intra-articular - intra-articular.
Modelele de osteoartroză induse fizic și chimic sunt în prezent foarte populare, dar reflectă procesele observate în osteoartroza secundară la om, mai degrabă decât osteoartroza idiopatică. O alternativă la acestea sunt modelele de osteoartroză spontană la primatele bipede și patrupede.
Unii autori sunt destul de sceptici în ceea ce privește modelarea osteoartrozei la animale în general. Astfel, conform lui MEJ Billingham (1998), utilizarea modelelor pentru descoperirea de medicamente modificatoare de osteoartroză este „...un joc de noroc costisitor”.
Modele de osteoartrită spontană
Aproape toate tulpinile de șoareci consangvinizați dezvoltă osteoartroză de severitate și localizare variabile. Cea mai mare incidență a osteoartrozei și cea mai severă evoluție a bolii se observă la șoarecii din tulpinile STR/ORT și STR/INS. Printre șoarecii STR/ORT, boala este mai frecventă și este mai severă la masculi decât la femele. Lezarea primară a cartilajului articular se dezvoltă în partea medială a plăcii tibiale. S-a presupus că apariția modificărilor cartilajului este precedată de deplasarea rotulei, însă RG Evans și colab. (1994), C. Collins și colab. (1994) au descoperit că la toți șoarecii din această tulpină, leziunea cartilajului se dezvoltă până la vârsta de 11 luni, dar nu toți au prezentat deplasarea rotulei. Aceiași autori au descoperit că modificările cartilajului articular la șoarecii STR/ORT sunt adesea precedate de metaplazia condrocito-osteoblastică a celulelor tendinoase și ligamentare din jurul articulațiilor genunchiului afectate, indicând faptul că aceste modificări sunt primare în patogeneza osteoartritei în acest model. Este posibil ca calcificarea inițială a ligamentelor și tendoanelor să modifice stresul mecanic asupra structurilor intraarticulare și ca modificările ulterioare ale cartilajului articular să reflecte o încercare de a menține o încărcare articulară normală. Spre deosebire de modelele de cobai și macac, în care degenerarea cartilajului este precedată de modificări ale osului subcondral, scleroza subcondrală apare mai târziu la șoarecii STR/ORT și STR/INS.
Avantajul acestui model de osteoartroză constă în dimensiunile reduse ale animalelor, care necesită un consum minim al agentului farmacologic testat. Cu toate acestea, dimensiunea este, de asemenea, un dezavantaj, deoarece analiza biochimică și patohistologică a cartilajului la șoareci este dificilă.
Studiile realizate de AM Bendele, JE Hulman (1988), AM Bendel și colab. (1989) și SCR Meacock și colab. (1990) dedicate studiului cursului natural al osteoartrozei spontane la cobai au stimulat interesul pentru acest model al bolii. Începând cu vârsta de 13 luni, toți cobaii masculi Dunkin Hurtley dezvoltă degenerare a cartilajului articular. Modificări similare la femele apar ceva mai târziu și sunt mai ușoare. La vârsta de 1 an, se observă pierderea completă a cartilajului articular în regiunea condilului medial al femurului și a plăcii tibiale. O creștere a greutății corporale la cobaii Dunkin Hurtley agravează cursul bolii, iar o scădere a greutății corporale la 900 g sau mai puțin îmbunătățește cursul osteoartrozei. La vârsta de 8 săptămâni, modificările osului subcondral sunt deja detectate în acest model, adică acestea din urmă preced deteriorarea cartilajului. Modificările ligamentelor încrucișate ale articulațiilor genunchiului pot accelera remodelarea osoasă.
Osteoartroza spontană se dezvoltă la macacii rhesus și cynomolgus. Un avantaj foarte important al primatelor față de alte animale folosite pentru a crea un model experimental de osteoartroză este bipedismul lor. Boala se dezvoltă la indivizii de vârstă mijlocie/vârstnici. Constatările histologice precoce includ îngroșarea osului subcondral urmată de uzura cartilajului articular în regiunea plăcii mediale a tibiei. Ulterior, placa laterală este implicată și ea în proces. În mod notabil, degenerarea cartilajului articular începe să se dezvolte numai după ce grosimea osului subcondral atinge 400 μm. Prevalența și severitatea osteoartrozei la macaci cresc odată cu vârsta, dar acești indicatori nu sunt afectați de sex și greutatea corporală. Până în prezent, modelele de osteoartroză la primate nu au fost utilizate pentru a studia eficacitatea DMOAD-urilor.
Modele de osteoartrita indusă fizic (chirurgical)
Modelele de osteoartrită bazate pe laxitatea genunchiului indusă chirurgical, care modifică stresul mecanic asupra articulației genunchiului, sunt cel mai frecvent utilizate la câini și iepuri. Cel mai utilizat model este cel cu transecția ligamentului încrucișat la câini. Modelele chirurgicale de osteoartrită la iepuri implică transecția ligamentelor încrucișate cu sau fără excizia ligamentelor mediale și colaterale, meniscectomie totală sau parțială și ruptură chirurgicală a meniscurilor. Au fost descrise modele chirurgicale de osteoartrită la cobai care implică transecția ligamentelor încrucișate și colaterale și meniscectomie parțială. Meniscectomia parțială la cobai are ca rezultat formarea de osteofite în decurs de 2 săptămâni și degenerarea excesivă a cartilajului articular în decurs de 6 săptămâni.
Până de curând, modelul canin de osteoartrită după transecția ligamentului încrucișat anterior a fost privit cu scepticism din cauza absenței ulcerațiilor cartilajului și a progresiei marcate a bolii observate în osteoartrita umană. JL Marshall și S. - E. Olsson (1971) au descoperit că modificările țesuturilor articulațiilor genunchiului la câini la 2 ani după operație au fost practic identice cu cele înregistrate imediat după operație. Autorii au sugerat că factorii mecanici (de exemplu, fibroza capsulei articulare și formarea de osteofite) stabilizează articulația genunchiului slăbită postoperator și previn progresia ulterioară a distrugerii cartilajului articular. De asemenea, s-a sugerat ca acest model să fie considerat un model de deteriorare și reparare a cartilajului, mai degrabă decât un model de osteoartrită. Cu toate acestea, rezultatele studiilor efectuate de KD Brandt și colab. (1991), care au studiat dinamica modificărilor țesuturilor articulațiilor genunchiului destabilizate de intersecția ligamentelor încrucișate anterioare pentru o perioadă mai lungă, au infirmat presupunerile autorilor anteriori.
SA McDevitt și colab. (1973, 1977) au constatat că deja în primele zile după transecția ligamentelor încrucișate, sinteza proteoglicanilor de către condrocitele cartilajului articular crește. Timp de 64 de săptămâni după inducerea chirurgicală a instabilității articulației genunchiului, grosimea cartilajului articular a fost mai mare decât în mod normal, deși modificările biochimice, metabolice și histologice ale acestuia au corespuns cu cele din osteoartroză. Această îngroșare a cartilajului a fost asociată cu o sinteză crescută a proteoglicanilor și cu concentrația mare a acestora în cartilajul articular. Folosind imagistica prin rezonanță magnetică (IRM), ME Adams și KD Brandt (1991) au arătat că după transecția ligamentelor încrucișate, hipertrofia cartilajului se menține timp de 36 de luni, apoi are loc o pierdere progresivă a cartilajului, astfel încât după 45 de luni majoritatea suprafețelor articulare sunt lipsite de cartilaj. Examinarea morfologică a cartilajului la 54 de luni după operație a confirmat constatările IRM. Astfel, ME Adams și KD Brandt (1991) au demonstrat că instabilitatea articulațiilor sufocate indusă chirurgical la câini poate fi considerată un model de osteoartrită.
Fenomenul reparării hipertrofice a cartilajului articular este bine ilustrat de modelul de osteoartroză la câini descris mai sus. Cu toate acestea, se știe că acest fenomen nu este specific acestuia. Hipertrofia cartilajului articular, care avea un caracter reparator, a fost descrisă pentru prima dată la pacienții cu osteoartroză de către EGL Bywaters (1937), iar mai târziu de LC Johnson. Se regăsește și în alte modele de osteoartroză - la iepuri după meniscectomie parțială (Vignon E. și colab., 1983), la macacii rhesus, hipertrofia cartilajului se dezvoltă spontan.
Descrierile moderne ale patogenezei se concentrează în principal pe „pierderea” progresivă a cartilajului, dar autorii trec adesea cu vederea îngroșarea acestuia și creșterea sintezei de proteoglicani, ceea ce corespunde fazei homeostatice a osteoartrozei stabilizate. În această fază, repararea cartilajului compensează pierderea acestuia și poate menține articulația într-o stare funcțională pentru o lungă perioadă de timp. Însă țesutul reparator adesea nu poate face față sarcinii mecanice impuse asupra sa în același mod ca și cartilajul articular sănătos, ceea ce duce la incapacitatea condrocitelor de a menține compoziția normală a matricei și la o scădere a sintezei de proteoglicani. Se dezvoltă stadiul final al osteoartrozei.
Studiul artropatiei Charcot a condus la dezvoltarea unei metode de accelerare neurogenă a modelării osteoartrozei induse chirurgical. Artropatia Charcot se caracterizează prin distrugere articulară severă, „șoareci” articulare, revărsat articular, instabilitate ligamentară și formarea de țesut osos și cartilaginos nou în cadrul articulației. Conceptul general al patogenezei artropatiei Charcot (neurogene) este întreruperea semnalelor senzoriale de la proprioceptorii și nociceptorii membrelor către sistemul nervos central (SNC). Pentru a accelera progresia osteoartrozei induse de transecția ligamentelor încrucișate anterioare la câini, se efectuează ganglioectomie sau excizia nervului care inervează articulația înainte de intervenția chirurgicală, ceea ce duce la apariția eroziunilor cartilajului deja în prima săptămână după intervenția chirurgicală. Interesant este că noua diacereină DMOAD a fost eficientă atunci când a fost utilizată într-un model de osteoartrită lent progresivă (neurologic intactă), dar a fost ineficientă în osteoartrita experimentală accelerată neurogenic.
În concluzie, trebuie menționat că este imposibil să se evalueze pe deplin identitatea modelului experimental de osteoartroză și osteoartroză la om, deoarece etiologia și mecanismele precise ale patogenezei bolii nu au fost încă clarificate. După cum s-a menționat anterior, scopul principal al utilizării modelelor experimentale de osteoartroză la animale este de a le utiliza pentru a evalua eficacitatea noilor medicamente, în principal din grupul „modificator al bolii”. Probabilitatea ca rezultatele tratamentului la un animal să coincidă cu rezultatele utilizării unui agent farmacologic experimental la om este, de asemenea, imposibil de determinat. N. S. Doherty și colab. (1998) au subliniat diferențele semnificative dintre speciile de animale utilizate pentru a modela osteoartroza în ceea ce privește dezvoltarea diferită a patologiei, diverși mediatori, receptori, enzime, ceea ce duce la o extrapolare obiectivă a activității terapeutice a noilor medicamente utilizate la animale la om. Un exemplu este eficacitatea ridicată a AINS în modelarea artritei inflamatorii la rozătoare. Acest lucru a condus la o reevaluare a eficacității AINS la om, la care prostaglandinele nu joacă rolul fundamental în patogeneza bolii pe care îl au la rozătoare, iar eficacitatea clinică a AINS este limitată la tratamentul simptomelor, mai degrabă decât la modificarea bolii.
În același timp, subestimarea noilor agenți farmacologici atunci când se studiază eficacitatea lor pe modele animale poate duce la pierderea unor agenți terapeutici potențial eficienți la om. De exemplu, sărurile de aur, penicilamina, clorochina și sulfasalazina, care au un anumit efect în tratamentul artritei reumatoide, sunt absolut ineficiente la animalele utilizate pentru screening-ul medicamentelor antireumatice.
Diferența de răspuns la tratamentul cu DMOAD între un model animal de osteoartroză și un pacient cu osteoartroză depinde în mare măsură de colagenază, o enzimă despre care se crede că este implicată activ în patogeneza osteoartrozei. Inhibitorii colagenazei interstițiale (colagenază-1 sau metaloproteinază matriceală (MMP)-1) se găsesc adesea la rozătoarele cu model OA, dar un omolog al colagenazei-1 umane nu a fost găsit la rozătoare și este posibil să nu existe. Astfel, inhibitorii specifici ai colagenazei-1 umane nu vor prezenta eficacitate terapeutică la rozătoarele cu osteoartroză experimentală. Majoritatea inhibitorilor MMP creați până în prezent sunt neselectivi și, prin urmare, inhibă colagenaza-3 (MMP-13), care este implicată în patogeneza osteoartrozei experimentale la rozătoare. Mai mult, așa cum au arătat studiile realizate de NRA Beeley și colab. (1994), JMP Freije și colab. (1994), colagenaza-3 umană este exprimată în cartilajul articular al pacienților cu osteoartroză și poate juca un rol în patogeneza bolii.
Se poate presupune că acești mediatori, receptori sau enzime joacă un rol similar în patogeneza osteoartrozei modelate la un anumit animal și la om. Un exemplu este capacitatea chemotactică a leucotrienei B4, care este considerată aceeași la om, șoareci și iepuri, dar activitatea antagoniștilor acestei substanțe biologic active diferă de 1000 de ori între speciile de animale. Pentru a evita astfel de inexactități în experimente, este necesar să se creeze metode care să permită studierea farmacodinamicii in vivo. De exemplu, este posibil să se studieze efectul oricăror substanțe asupra activității enzimelor sau mediatorilor exogeni la om. Această tehnică a fost utilizată de V. Ganu și colab. (1994) pentru a evalua activitatea inhibitorilor MMP prin determinarea capacității medicamentelor de a inhiba eliberarea proteoglicanilor din cartilajul articular după injectarea de stromelesină umană în articulația genunchiului unui iepure.
Deși rezultatele obținute în modelul experimental de osteoartroză pot duce la o evaluare incorectă a potențialelor DMOAD-uri, modelele animale de osteoartroză joacă un rol important în cercetarea fundamentală. O decizie finală privind eficacitatea agenților farmacologici în tratamentul bolilor umane poate fi luată numai după efectuarea studiilor clinice de fază III la om.


 [
[