Expert medical al articolului
Noile publicații
Gliom al creierului
Ultima examinare: 07.06.2024

Tot conținutul iLive este revizuit din punct de vedere medical sau verificat pentru a vă asigura cât mai multă precizie de fapt.
Avem linii directoare de aprovizionare stricte și legătura numai cu site-uri cu reputație media, instituții de cercetare academică și, ori de câte ori este posibil, studii medicale revizuite de experți. Rețineți că numerele din paranteze ([1], [2], etc.) sunt link-uri clickabile la aceste studii.
Dacă considerați că oricare dintre conținuturile noastre este inexactă, depășită sau îndoielnică, selectați-o și apăsați pe Ctrl + Enter.
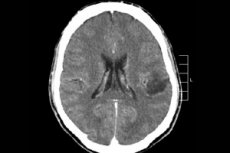
Printre numeroasele procese tumorale ale sistemului nervos central, gliomul creierului este cel mai adesea diagnosticat - acest termen este colectiv, neoplasmul combină toate focarele oligodendrogliale și astrocitic difuze, astrocitom, astroblastom și așa mai departe. O astfel de tumoră poate avea un grad diferit de malignitate, este format din structuri gliale - celule localizate în jurul neuronilor. Principala zonă de localizare a glioamelor sunt emisferele cerebrale, pereții ventriculelor creierului și chiasma - zona intersecției parțiale a fibrelor nervoase optice. Extern, tumora este un element nodular de nuanță roz sau roșiatică, configurație rotundă sau în formă de fus, cu limite indistinse. [1]
Epidemiologie
În aproximativ 5% din cazuri, gliomele sunt asociate cu patologii ereditare - în special, neurofibromatoză și alte sindroame cu moștenire dominantă. Experții subliniază că majoritatea absolută a gliomelor cerebrale se dezvoltă sporadic - adică fără o cauză clară.
În general, neoplasmele primare ale sistemului nervos central reprezintă aproximativ 2% din toate tumorile, sau puțin peste 21 de cazuri la sută de mii de populație. Printre ele, gliomele apar în 35-36% din cazuri, iar mai mult de 15% dintre ele sunt glioblastoame.
Conform unor date, gliomul afectează bărbații mai des decât femeile - tumora este deosebit de frecventă în rândul persoanelor de peste 50 de ani.
Incidența globală a glioamelor în rândul vârstnicilor a crescut semnificativ în ultimele decenii. Motivele acestui fenomen nu au fost încă stabilite.
Conform definiției Organizației Mondiale a Sănătății, au fost identificate trei variante principale ale tumorilor gliale, care diferă în caracteristicile lor histologice. Acestea sunt oligodendrogliomele, astrocitomele și oligoastrocitomele combinate. Incidența fiecărui subtip de patologie malignă scăzută nu a fost determinată în mod fiabil. Unele studii indică o creștere a incidenței oligodendrogliomelor de la 5% la 30% și o scădere a incidenței astrocitomelor.
Tumorile gliale sunt capabile să infiltreze țesutul creierului, iar marea majoritate a focarelor de grad scăzut devin maligne în câțiva ani. [2]
Cauze Glioame cerebrale
Gliomul creierului este un grup întreg de procese tumorale, a căror caracteristică comună este formarea lor din structurile gliale ale SNC localizate în țesutul creierului. Astfel de tumori sunt împărțite în două variante histopatologice: glioame maligne ridicate și scăzute.
Sursa de formare a creșterii este celulele Neuroglia (astrocite, oligodendrocite), care oferă baza structurală și viabilitatea neuronilor creierului.
Procesele tumorale gliale diferă foarte mult în structură, modificări mutaționale ale genelor, agresivității, caracteristicilor clinice, caracteristicilor de diagnostic, răspunsului la tratament și prognosticului pacienților. Neoplasmele embrionare și ependimale ale sistemului nervos central - în special, medulloblastoame și ependimome - diferă în structura lor histologică, dar sunt similare în ceea ce privește tratamentul.
Elementele gliale au fost clasificate pentru prima dată ca o categorie structurală separată a sistemului nervos la sfârșitul secolului al XIX-lea.
Țesutul Neuroglia este format din celule care au funcții auxiliare: trofic, suport, protector, secretor. Neuronii și gliocitele există împreună cu celălalt, ei formează împreună sistemul nervos și au o importanță deosebită în procesele generale ale activității vitale a organismului.
Gliocitele sunt clasificate aproximativ în mai multe forme majore: astrocite, oligodendrocite, celule ependimale și microglie.
Până în prezent, oamenii de știință nu pot răspunde la întrebarea cu privire la cauzele fiabile ale formării tumorii neurogliale. Se presupune că o anumită contribuție negativă este făcută prin efecte radioactive, boli infecțioase, intoxicație (în special chimică, ocupațională). Factorul ereditar este, de asemenea, important.
Gliomele creierului apar din neurogliocite anormale care au un defect genetic care duce la o creștere și funcționalitate anormală - astfel de structuri sunt denumite „imaturi”. Celulele incomplete sunt mai des localizate într-o zonă, unde se formează tumora.
Mai simplu spus, formarea glială este rezultatul creșterii haotice și sporadice a celulelor neuroglii modificate. Procesul se poate dezvolta din ependimocite, oligodendrocite, astrocite (astrocitom, inclusiv celule uriașe și anaplastice). [3]
Factori de risc
În ciuda faptului că experții nu pot caracteriza cu exactitate cauzele formării oncopatologiilor gliale, în unele cazuri aspectul lor poate fi prevenit prin eliminarea principalilor factori de risc:
- Expunerea la radiații ionizante are activitate cancerigenă, poate provoca dezvoltarea leucemiei și formarea proceselor de cancer cu o structură densă, inclusiv la persoane de vârstă fragedă. Proceduri medicale radiologice frecvente și nerezonabile, radiațiile ultraviolete (inclusiv solariul) aparțin, de asemenea, efectelor cancerigene potențiale și pot provoca apariția tumorilor în diferite organe, inclusiv creierul.
- Efecte adverse profesionale, intoxicațiile au adesea o legătură cauzală cu dezvoltarea tumorilor canceroase. Producția de cauciuc și sticlă, pesticide și combustibili, metale și textile, vopsele și reactivi de laborator sunt considerate deosebit de periculoase. În pericol sunt lucrătorii din industria aerospațială, cărbune și metal, fabrici de fabricație chimică și subprodusă, materiale de construcție și electrozi, combustibili și lubrifianți, materiale plastice și monomeri.
- Poluarea aerului, a apei și a solului sunt responsabile pentru până la 4% din toate patologiile cancerului din lume. Carcinogenii, prezenți în cantități mari în mediu, intră în corp cu aer inhalat, apă potabilă și alimente. Trăind în zone ecologice nesigure - în apropierea unor mari instalații industriale, schimburi de transport aglomerate - este considerată deosebit de periculoasă.
- Patologii infecțioase - în special infecții virale - pot crea, de asemenea, condiții favorabile dezvoltării tumorilor. Este important să țineți cont de acest lucru și să fie vaccinați în avans, precum și pentru a preveni bolile infecțioase și parazite.
- Intoxicarea tutunului și a alcoolului sunt considerați factori de risc pentru multe soiuri de cancer, nu doar gliomele creierului.
- Activitate fizică insuficientă, supraponderală, nutriție necorespunzătoare, tulburări metabolice, leziuni la cap, patologii vasculare - factori de stres suplimentari care pot provoca începerea tulburărilor intracelulare.
- Vârsta mai mare este cea mai frecventă perioadă pentru dezvoltarea neoplasmelor în organism, astfel încât cei cu vârsta peste 55 de ani ar trebui să aibă grijă specială de propria sănătate.
Cu toate acestea, principalul și cel mai semnificativ factor de risc pentru dezvoltarea gliomului rămâne predispoziție ereditară.
Patogeneza
Până în prezent, experții au o serie de presupuneri cu privire la dezvoltarea gliomelor cerebrale. Fiecare teorie are propriile sale motive, dar singurele oameni de știință patogenetici corecți și fiabili nu au fost încă identificați. În cele mai multe cazuri, vorbim despre următorii factori în dezvoltarea neoplasmelor:
Eșecul embriogenezei, care constă în perturbarea depunerii de organe și în formarea structurilor celulare „greșite”;
- Expunerea la raze ionizante, cancerigeni potențiali sub formă de agenți chimici, aditivi alimentari, etc.;
- Trauma capului;
- Tulburările genice transmise de la generație la generație (gliom „familial”);
- Disfuncție imună, neuroinfecții.
Majoritatea glioamelor au o creștere difuză, cu penetrarea în țesutul creierului normal înconjurător. În funcție de gradul de malignitate, tumora se poate dezvolta timp de câțiva ani fără nicio manifestare. În cazul unui curs agresiv, simptomatologia crește rapid pe parcursul mai multor luni.
O parte din tumorigeneză se datorează modificărilor dismbriogenetice.
Brainstemul poate fi afectat la diferite niveluri: la rândul său, gliomul difuz al trunchiului cerebral va diferi atât anatomo-morfologic, cât și clinic. Unele astfel de neoplasme - în special, gliomul plăcii quadriplegie - pot fi relativ benigne, fără semne de progresie. Pe de altă parte, un gliom pontin este caracterizat prin malignitatea sa particulară, agresivitatea și prognosticul slab.
Leziuni difuze ale structurilor creierului, în care mai mult de trei zone anatomice ale emisferelor mari sunt implicate în procesul patologic, cu o posibilă divergență periventriculară și trecere prin Gliomatoza numită Gliomatoză. [4]
Este ereditară glioma creierului?
Un risc bine dovedit de formare a gliomului cerebral este ereditară - adică prezența tumorilor similare sau alte intracerebrale în strămoși directe sau în aceeași generație. Expunerile radioactive și contactul regulat sau prelungit cu cancerigenii potențiali agravează situația.
Nu numai că gliomele pot fi moștenite, dar și boli care sunt însoțite de creșterea creșterii tumorii, fără a face referire la localizare-în special, aceasta poate fi neurofibromatoza tip 1 și 2, sindromul Li-Fraumeni, Hippel-Lindau. Adesea în celulele gliomului, sunt detectate modificări ale anumitor gene sau cromozomi.
Principalele patologii care sunt asociate cu dezvoltarea gliomului la om sunt rezumate în tabel:
Patologie |
Cromozom |
Gene |
Varietate de neoplasmă |
Sindromul Li-Fraumeni |
17р13 |
TR53 |
Neoplasme neuroectodermice, astrocitom. |
Neurofibromatoză |
17q11 |
NF1 |
Gliom nervos optic, astrocitom pilocitic, neurofibromatoză |
Sindromul Turcotte |
3p21, 7p22 |
HMLH1, HPSM2 |
Astrocitom |
Scleroză tuberculoasă (sindromul Burneville). |
9Q34, 16P13 |
TSC1, TSC2 |
Astrocitom subependimal gigantocelular |
Indiferent de natura tumorii gliale, indiferent dacă este un caz sporadic sau o patologie ereditară, este o tulburare cu expresia unei gene modificate patologic. În afară de neoplasme formate ca urmare a efectelor de învățare, în alte situații, cauzele modificărilor genetice rămân neclare.
Simptome Glioame cerebrale
Caracteristicile simptomatologiei focale depind direct de zona de localizare a gliomului cerebral și devin o consecință a tot felul de tulburări endocrine, compresia țesutului nervos sau a proceselor distructive locale.
Dacă neoplasmul este localizat în zona parietală, atunci o persoană este dominată de astfel de manifestări precum convulsii, tulburări senzoriale, deficiențe de auz.
Când gliomul este localizat în zona emisferei dominante, sunt detectate tulburări de vorbire, agrafia, agnozia.
Neoplasmele cu lobul temporal sunt adesea însoțite de convulsii convulsive, afazie, sensul mirosului și funcției vizuale și dispnee.
Când presiunea intracraniană crește, o imagine corespunzătoare se dezvoltă cu restricția câmpurilor vizuale, paralizia mușchilor oculari și hemiplegia.
Datorită specificității procesului tumoral, gliomul cerebral este întotdeauna însoțit de simptome neurologice într-o măsură mai mare sau mai mică. La început, există o slăbiciune generală vizibilă, pacientul dorește constant să doarmă, capacitatea de a lucra este afectată, procesele de gândire sunt încetinite. În această etapă, există un risc ridicat de a face un diagnostic incorect și, în consecință, de a prescrie un tratament greșit. Printre alte manifestări nespecifice:
- Tulburări vestibulare, inclusiv mersul nesigur, pierderea echilibrului (de exemplu, la bicicleta sau scările de urcare), amorțeală la membre, etc;
- Deteriorarea treptată a vederii, dublarea imaginii vizuale;
- Deteriorarea funcției auditive;
- Discurs înclinat;
- Greață și vărsături sub formă de atacuri independente de alimente sau băuturi;
- Slăbirea mușchilor mimici și a altor mușchi faciali;
- Disconfort atunci când înghiți;
- Dureri de cap obișnuite (adesea în orele de dimineață).
Imaginea clinică se extinde treptat și se agravează: la unii pacienți se întâmplă lent, în alții - brusc, literalmente „în fața ochilor”, în câteva săptămâni. În ultimul caz, vorbim despre un gliom agresiv, în curs de dezvoltare rapidă a creierului.
Primele semne
Gliomul creierului în primele etape ale dezvoltării nu are o simptomatologie pronunțată. Primele manifestări sunt adesea confundate cu semne ale altor patologii mai puțin periculoase.
În general, imaginea clinică a gliomului este diversă și este determinată de locația și dimensiunea focalizării patologice. Pe măsură ce neoplasmul crește, simptomele cerebrale generale se dezvoltă și cresc:
- Dureri persistente și obișnuite ale capului care nu răspunde la medicamentele standard (medicamente antiinflamatoare nesteroidiene);
- Greață intermitentă, uneori până la punctul de vărsături;
- O senzație incomodă și grea în zona globului ocular;
- Convulsii.
Manifestările cerebrale sunt deosebit de intense atunci când tumora crește în ventricule sau în sistemul de lichior. Drenajul lichidului cefalorahidian este afectat, crește presiunea intracraniană și se dezvoltă hidrocefalie. Procesul afectează o anumită parte a creierului, care afectează dezvoltarea clinicii corespunzătoare:
- Există probleme cu funcția vizuală;
- Discursuri de vorbire;
- Apar tulburări vestibulare (amețeli, coordonare afectată a mișcărilor);
- Pareză, paralizie a brațelor, picioarelor;
- Memoria și concentrarea sunt afectate;
- Procesele de gândire sunt afectate;
- Tulburările comportamentale apar.
În stadiul inițial, simptomele sunt practic absente sau sunt atât de nesemnificative încât nu atrag atenția. Din acest motiv, experții sfătuiesc cu tărie examinările și verificările preventive periodice. La urma urmei, este detectat mai devreme procesul tumorii, cu atât sunt mai mari șansele de vindecare și supraviețuire. [5]
Gliomul creierului la un copil
Printre numeroasele tumori cerebrale găsite în copilărie, procentul de gliome variază de la 15 la 25%. Copiii pot obține boala la adolescența lor timpurie și la începutul anilor 20, deși este foarte rar pentru bebelușii sub 3 ani să obțină boala.
Patologia începe pe fundalul mutației celulelor gliale. Până în prezent, nu există niciun răspuns la întrebarea de ce are loc această mutație.
Singurul lucru care a fost învățat în mod fiabil este faptul că anumite boli moștenite asociate cu un risc crescut de creștere a tumorii cresc probabilitatea dezvoltării și a dezvoltării gliomului cerebral.
În plus, oamenii de știință au descoperit că celulele gliale pot avea divergență în gene individuale sau cromozomi. Din cauza acestei tulburări, un mecanism de mutație intră, ceea ce nu este ereditar. Este posibil ca acest lucru să se întâmple la una dintre primele etape ale dezvoltării.
Este un fapt dovedit că prezența leucemiei acute sau retinoblastomului în istoria copilului sau iradierea creierului din orice alt motiv, crește semnificativ riscurile de formare a gliomului (după o anumită perioadă de timp).
Simptomatologia în copilărie depinde de gradul de malignitate și localizarea focalizării patologice. Se face o distincție între simptomele specifice și nespecifice:
- Simptomele nespecifice nu sunt „legate” de zona în care se află gliomul. Manifestările comune pot include dureri de cap, amețeli, apetit slab, vărsături fără legătură cu aportul alimentar, pierderea în greutate (din motive necunoscute), senzația constantă de oboseală, scăderea performanței academice, dificultăți în concentrare, tulburări de comportament. Aceste semne se datorează compresiei structurilor intracraniene, care pot fi explicate ca o presiune directă a masei în creștere și o tulburare în circulația lichidului cefalorahidian. Există riscul de hidrocel cerebral.
- Simptomatologia specifică depinde de locația imediată a focalizării patologice gliale. De exemplu, tumora cerebeloasă este de obicei însoțită de mersul afectat și echilibrul la copii. Leziunea creierului mare se manifestă prin convulsii convulsive și creșterea tumorii în paralizia măduvei spinării - a musculaturii. Se întâmplă ca viziunea bebelușului să se deterioreze brusc, conștiința este perturbată, somnul este afectat sau apare o altă problemă de dezvoltare.
De regulă, în copilărie, gliomul malign se dezvăluie în câteva săptămâni sau luni de dezvoltare: adesea caracterizat prin creșterea rapidă și necontrolată a neoplasmului.
Copiii cu tumori gliale maligne sunt tratați de medici la centrele clinice pediatrice specializate în oncologie pediatrică. De regulă, se utilizează cursuri chirurgicale, radiații și chimioterapie.
Cea mai importantă etapă de tratament este neurochirurgia. Cu cât este mai radicală, cu atât sunt mai bune șansele copilului pentru o cură. Dar intervenția chirurgicală nu este întotdeauna posibilă: în special, pot apărea probleme odată cu îndepărtarea glioamelor din trunchiul cerebral, precum și cu radiațiile pentru copiii sub 3 ani.
Gliomele creierului central (intermediar și creier de mijloc) sunt dificil de îndepărtat complet, deoarece există riscul de deteriorare a țesutului sănătos. Dacă rezecția completă a tumorii este imposibilă, pacientului i se prescrie tratament paliativ.
Copiii cu gliome maligne sunt tratați în conformitate cu protocoalele standardizate care au fost determinate prin studii clinice controlate riguros. Cele mai frecvente protocoale sunt următoarele:
- HIT HGG 2007: implică tratamentul copiilor cu vârste cuprinse între 3-17 ani.
- Hit SKK: Potrivit pentru sugari (până la trei ani) și nu implică tratamente cu radiații.
Statisticile de supraviețuire pediatrică pentru gliomuri nu sunt în general foarte optimiste. Cu toate acestea, în niciun caz nu este posibil să prezicem în avans eficacitatea măsurilor de tratament pentru un anumit copil. Este important să urmați cu atenție toate ordinele medicului, ceea ce crește semnificativ șansele de recuperare.
Formulare
Gliomele pot fi scăzute maligne și maligne ridicate, cu o creștere intensă și o tendință de metastazare. Este important să înțelegem că malignitatea scăzută nu este sinonimă cu siguranța tumorii. Orice neoplasm cerebral creează un volum suplimentar, stoarce structuri cerebrale, ceea ce duce la deplasarea lor și la creșterea presiunii intracraniene. Drept urmare, pacientul poate muri.
Există două tipuri principale de astrocitome maligne. Acestea sunt glioblastomele și astrocitomele anaplastice, care sunt subdivizate în funcție de modificările moleculare. Tumorile maligne secundare care s-au dezvoltat din astrocitome și au un grad scăzut de malignitate se găsesc cel mai adesea la pacienții tineri. Inițial tumorile de tip glial malign apar mai des la pacienții vârstnici.
În funcție de locația structurală, gliomele intră:
- Supratentorial (cu localizare deasupra cerebelului în zona ventriculelor laterale, emisfere mari);
- Subtentorial (cu localizare sub cerebel în fosa craniană posterioară).
Conform caracteristicilor histologice, distinge astfel de tipuri de gliome:
- Gliomul astrocitic este cel mai frecvent. La rândul său, este împărțit în nodular și difuz (acesta din urmă poate fi caracterizat prin creștere rapidă și un model de accident vascular cerebral).
- Oligodendrogliom - apare la 5% dintre pacienți. Are petrificate - zone de calcifiere, cel mai adesea în lobul frontal.
- Gliomul ependimal - crește din structurile care aliniază pereții canalului central al măduvei spinării și ventriculelor. Adesea crește în grosimea substanței creierului, precum și în lumenul creierului.
Sunt posibile și focare patologice mixte, cum ar fi subependimomul, oligoastrocitom, etc.
Toate gliomele sunt clasificate în următoarele etape:
- Neoplasme relativ benigne cu creștere lentă, fără simptome clinice evidente.
- Gliomele „de frontieră” cu creștere lentă care se transformă treptat în stadiul III și nu numai.
- Gliom malign.
- Gliom malign cu o creștere agresivă intensă și răspândire, cu prognostic slab.
Cu cât este mai mică stadiul de malignitate, cu atât este mai mică probabilitatea de metastaze și reapariția neoplasmei îndepărtate și cu atât sunt mai mari șansele de vindecare a pacientului. Cel mai mare pericol este prezentat de Glioblastoma Multiforme, un proces cu diferență scăzută, cu creștere și dezvoltare intensă. [6]
Posibile și cele mai frecvente variante ale neurogliomului:
- Glioma cu creier și leziuni pontine este localizat în zona în care creierul se conectează la măduva spinării. Există că neurocentii importanți responsabili de funcția respiratorie, cardiacă și motorie sunt localizate. Dacă această zonă este deteriorată, munca vestibulară și aparatul de vorbire este perturbată. Este adesea detectat în copilărie.
- Gliomul vizual afectează celulele neurogliale care înconjoară nervul optic. Patologia provoacă deficiențe de vedere și exoftalm. Se dezvoltă mai des la copii.
- Neurogliomul malign scăzut se caracterizează prin creșterea lentă, localizată mai des în emisferele mari și cerebelul. Apare mai des la tineri (adolescenți și adulți tineri în jur de 20 de ani).
- Gliomul corpus callosum este mai caracteristic persoanelor între 40 și 60 de ani și este cel mai frecvent reprezentat de glioblastom.
- Gliomul Chiasma este localizat în zona de joncțiune optică, deci este însoțită de miopie, pierderi de câmp vizual, hidrocefalie ocluzivă și tulburări neuroendocrine. Poate apărea la orice vârstă, dar cel mai frecvent afectează pacienții cu neurofibromatoză de tip I.
Complicații și consecințe
Gliomele de malignitate scăzută (gradul I-II, extrem de malign - de exemplu, astrocitom, oligoastrocitom, oligodendrogliom, xantrocitom pleomorf Gliomele de gradul IV sunt deosebit de maligne.
Gliomul trunchiului cerebral are un prognostic foarte nefavorabil tocmai pentru că neoplasmul afectează o astfel de regiune a creierului, unde cele mai importante conexiuni nervoase dintre creier și membre sunt concentrate. Chiar și o tumoră destul de mică în această zonă este suficientă pentru a face ca starea pacientului să se deterioreze rapid și să provoace paralizia.
Nu mai puțin nefavorabile consecințe atunci când sunt afectate alte regiuni ale creierului. Adesea, este o tumoră a cortexului cerebral, care nu oferă o șansă pentru o lungă speranță de viață a pacientului, în ciuda tratamentului. Adesea este posibil să amânați moartea.
Conform statisticilor medicale, rata de supraviețuire de cinci ani este adesea de doar 10-20%. Deși aceste cifre depind în mare parte de gradul de malignitate, cât și de localizarea exactă și de volumul intervenției chirurgicale efectuate. După îndepărtarea completă a focalizării patologice, rata de supraviețuire crește semnificativ (uneori - până la 50%). Lipsa de tratament sau imposibilitatea acestuia (dintr-un motiv sau altul) este garantată să conducă la moartea pacientului.
Majoritatea tumorilor gliale maligne scăzute sunt capabile să infiltreze țesutul creierului și să malignizeze de-a lungul mai multor ani.
Riscul de reapariție a gliomului este considerat de experți drept „extrem de probabil”. Cu toate acestea, tratamentul nu trebuie neglijat: este important să vă asigurați o calitate bună a vieții cât mai mult timp posibil.
Gliomele recurente au întotdeauna un prognostic mai rău decât tumorile primare. Cu toate acestea, protocoalele moderne de tratament bazate pe studiile de optimizare terapeutică obțin adesea rezultate suficient de bune pentru pacienții chiar și cu neoplasme extrem de maligne.
Posibile rezultate după chimioterapie:
- Emaciarea, emaciarea, tulburările digestive, bolile orale;
- Excitabilitatea crescută a sistemului nervos central, astenia;
- Deteriorarea funcției auditive, tinitus și sună în urechi;
- Convulsii, tulburări depresive;
- Criză hipertensivă, schimbarea modelului de sânge;
- Insuficiență renală;
- Procese alergice, căderea părului, aspectul petelor de pigment pe corp.
După chimioterapie, pacienții notează o slăbire pronunțată a sistemului imunitar, ceea ce poate provoca dezvoltarea diferitelor patologii infecțioase.
Diagnostice Glioame cerebrale
Un gliom cerebral poate fi suspectat prin următoarele semne:
- Pacientul are convulsii localizate sau generalizate, care sunt caracteristice locației corticale a neoplasmului și dezvoltării sale lente. Epiriizerile se găsesc la 80% dintre pacienții cu tumori gliale de grad scăzut și la 30% dintre pacienții cu gliome de înaltă calitate.
- Presiunea intracraniană crescută este caracteristică deosebit de mase situate în lobii frontali și parietali dreapta. Asociat cu tulburarea ridicată a presiunii intracraniene a circulației sângelui și a circulației lichiorului implică apariția durerii de cap constante și crescânde, greață cu vărsături, tulburări vizuale, somnolență. Există edem al nervului optic, paralizia nervului de deviere. O creștere a presiunii intracraniene la valorile critice poate duce la dezvoltarea comelor și a morții. O altă cauză a IOP ridicată este hidrocefalia.
- Pacientul are o imagine focală în creștere. În formațiunile supratentoriale, sferele motorii și senzoriale sunt perturbate, hemiopia, afazia și tulburările cognitive progresează.
Dacă medicul suspectează prezența unui neoplasm cerebral, este optim să se efectueze RMN fără sau cu introducerea agentului de contrast (Gadolinium) pentru a afla locația, dimensiunea și caracteristicile sale suplimentare. Dacă imagistica prin rezonanță magnetică nu este posibilă, se efectuează tomografia calculată și se folosește spectroscopia prin rezonanță magnetică ca metodă de diferențiere. În ciuda informativității acestor metode de diagnostic, diagnosticul final se face numai după confirmarea histologică în timpul rezecției concentrării tumorii.
Având în vedere criteriile de mai sus, se recomandă începerea diagnosticului cu un istoric minuțios, evaluarea stării somato-neurologice și a statutului funcțional. Starea neurologică este evaluată împreună cu determinarea tulburărilor intelectuale și mnestice probabile.
Testele de laborator recomandate:
- Un antrenament general de sânge clinic general;
- Un panou complet de chimie a sângelui;
- Analiza urinară;
- Studiu de coagulare a sângelui;
- Analiza pentru markerii oncologici (AFP, beta-hCG, LDH - relevant dacă este suspectată o leziune a zonei pineale).
Pentru a clarifica punctele prognostice la pacienții cu glioblastom și astrocitom anaplastic, sunt evaluate mutația genei IDH1 | 2-1 și metilarea genei MGMT. La pacienții cu oligodendrogliom și oligoastrocitom, se determină 1p | 19Q codlelație.
Diagnosticul instrumental, în primul rând, este reprezentat de imagistica de rezonanță magnetică obligatorie a creierului (uneori - și măduva spinării). RMN este efectuat în trei proiecții folosind moduri standard T1-2, fler, T1 cu contrast.
Când este indicat, ecografia rețelei vasculare, imagistica prin rezonanță magnetică funcțională a secțiunilor motorii și de vorbire, precum și angiografia, spectroscopia, tractografia MR și perfuzia.
Investigații suplimentare pot include:
- Electroencefalografia creierului;
- Consultări cu un neurochirurg, oncolog, radiolog, oftalmolog, radiolog.
Diagnostic diferentiat
Diagnosticul diferențial este efectuat în mod necesar cu patologii non-tumorale-în special, cu hemoragie cauzată de malformație arterio-venoasă sau arterială, precum și cu procese de demielinare pseudotumoră, boli inflamatorii (toxoplasmoză, abces cerebral etc.).
În plus, diferențiați focalizarea tumorii primare și metastazele sistemului nervos central.
Cu capacități de imagistică cu rezonanță magnetică modernă, este posibil să se efectueze măsuri de diagnostic suficient de exact, pentru a afla originea focalizării primare în SNC. RMN-ul creierului este efectuat cu sau fără contrast, în modul T1, T2 Flair - în trei proiecții sau felii subțiri în proiecție axială (modul SPGR). Aceste metode de diagnostic permit să determine cu exactitate locația, dimensiunea, caracteristicile structurale ale neoplasmului, relația sa cu rețeaua vasculară și zonele creierului din apropiere.
În plus, CT (cu sau fără contrast), angiografia CT (angiografia MR), tractografia MR, perfuzia MR sau CT pot fi efectuate ca parte a diagnosticului diferențial. CT/PET al creierului cu metionină, colină, tirozină și alți aminoacizi este utilizat atunci când este indicat.
Tratament Glioame cerebrale
Terapia specifică constă în măsuri chirurgicale, chimioterapeutice și radiații. Este obligatoriu, dacă este posibil, să efectuați o rezecție completă a focalizării tumorii, ceea ce permite ameliorarea rapidă a simptomelor și confirmarea histologică a diagnosticului.
Iradierea are un efect pozitiv asupra creșterii speranței de viață a pacienților. O doză totală de 58 până la 60 Gy, împărțită în doze individuale de iradiere de 1,8-2 Gy, este administrată ca standard. Tumora este iradiată la nivel local, captând în plus până la 3 cm în jurul ei. Radioterapia este mai acceptabilă, spre deosebire de brahiterapie. În unele cazuri, sunt recomandate metode radiochirurgicale, care constau în iradiere cu un cuțit gamma sau o pedală de gaz liniar, precum și o terapie cu bor-captură de neutroni.
Necesitatea chimioterapiei adjuvante este controversată. În unele cazuri, preparatele de nitrosourea au permis să crească speranța de viață a pacienților până la un an și jumătate, dar unele rezultate ale utilizării unor astfel de chimiopreparate au fost negative. Astăzi, agenții citotoxici, terapia neoadjuvantă (înainte de radiații), medicamente combinate, chimioterapie intra-arterială sau chimioterapie cu doze mari cu transplant de celule stem suplimentare sunt utilizate activ.
În general, pentru tratamentul cu succes al gliomelor, o abordare cuprinzătoare este foarte importantă, a căror amploare depinde de locația și gradul de malignitate a masei, dimensiunea și sănătatea generală a pacientului.
În legătură cu gliomul trunchiului cerebral, intervenția chirurgicală este rareori utilizată. Principala contraindicație a intervenției chirurgicale este zona de localizare a focalizării - în imediata apropiere a părților vitale. În unele cazuri, este posibilă eliminarea gliomului portbagajului folosind metode microchirurgicale, cu chimioterapie preoperatorie și postoperatorie. O astfel de intervenție este foarte complexă și necesită calificări speciale ale unui neurochirurg.
Chirurgia de radiații și, în special, o intervenție chirurgicală stereotactică cu expunere la doze ionizante ridicate este destul de eficientă. Utilizarea unei astfel de tehnici în stadii incipiente ale dezvoltării neoplasmei permite uneori să obțină o remisiune prelungită sau chiar o vindecare completă a pacientului.
Radiația este adesea combinată cu chimioterapia, ceea ce îmbunătățește eficacitatea intervențiilor și reduce sarcina radiațiilor. În gliome, nu toți agenții chimiopreventivi au succes terapeutic, astfel încât sunt prescriși individual, iar rețetele sunt ajustate, dacă este necesar.
Pentru a reduce durerea și a scădea presiunea intracraniană, indiferent de tratamentul principal, terapia simptomatică este prescrisă - în special, medicamente corticosteroide, analgezice, sedative.
Medicamente
Medicamentele corticosteroide afectează umflarea, reduc gravitatea simptomelor neurologice timp de câteva zile. Cu toate acestea, din cauza efectelor secundare multiple și a probabilității crescute a interacțiunilor adverse cu medicamentele chimioterapice, se utilizează doze minim eficiente de steroizi, întrerupându-le cât mai curând posibil (de exemplu, după operație).
Anticonvulsivanții sunt utilizați în mod sistematic ca măsură preventivă secundară la pacienții care au avut deja convulsii epileptice. Aceste medicamente pot provoca simptome adverse grave și, de asemenea, interacționează cu medicamentele chimioterapice.
Anticoagulantele sunt relevante în special în stadiul postoperator, deoarece riscurile formării tromboflebitelor în gliom sunt destul de mari (până la 25%).
Se așteaptă un efect bun de la luarea antidepresiei-anxiolitice. Utilizarea metilfenidatului 10-30 mg/zi în două doze permite adesea optimizarea abilităților cognitive, îmbunătățirea calității vieții, menținerea capacității de lucru.
Eșecul neurologic și semnele edemului cerebral (durerea în cap, tulburările conștiinței) sunt eliminate de medicamente corticosteroide - în special, prednisolon sau dexametazonă. |
Schema și doza de corticosteroizi este selectată individual, cu practica dozei minime eficiente. La sfârșitul cursului de tratament, medicamentele sunt retrase treptat. |
Corticosteroizii sunt luați împreună cu medicamente gastroprotectoare-blocante ale pompei de protoni sau H2-histaminăBlocanți. |
Diureticele (furosemidă, manitol) sunt prescrise pentru umflarea severă și deplasarea structurilor creierului, ca adjuvant la medicamentele corticosteroide. |
În cazul convulsiei convulsive (inclusiv anamneză) sau simptome epileptiforme pe electroencefalogramă, în plus, terapia anticonvulsivă este prescrisă. Anticonvulsivanții nu sunt prescriși în scopuri profilactice. |
Pacienții cu indicații pentru chimioterapie li se recomandă să ia anticonvulsivante care nu afectează funcția enzimei hepatice. Medicamente la alegere: lamotrigină, acid valproic, levetiracetam. Nu trebuie utilizat: carbamazepină, fenobarbital. |
Durerea capului în gliomele creierului este gestionată cu tratamentul cu corticosteroizi. |
În unele cazuri de dureri de cap, pot fi utilizate medicamente antiinflamatorii nesteroidiene sau tramadol. |
Dacă pacientul ia medicamente antiinflamatoare nesteroidiene, este întrerupt cu câteva zile înainte de operație pentru a minimiza șansa de sângerare în timpul operației. |
În cazurile de durere selectate, pot fi recomandate analgezice narcotice - cum ar fi fentanil sau trimeperidină -. |
Pentru a preveni embolia pulmonară de a treia zi postoperatorie, se prescriu administrarea de heparine cu greutate moleculară mică - în special, enoxaparină sodiu sau calciu de nadroparină -. |
Dacă pacientul se află pe un tratament anticoagulant sau antiagregant sistematic, el este transferat la heparine cu greutate moleculară scăzută cu cel mult o săptămână înainte de intervenția chirurgicală, cu retragerea lor suplimentară cu o zi înainte de operație și reluare la 24-48 de ore după operație. |
Dacă un pacient cu gliom are tromboză venoasă a extremităților inferioare, se efectuează tratament cu anticoagulante directe. Posibilitatea de a plasa un filtru cava nu este exclusă. |
Chimioterapie pentru gliomele maligne ale creierului
Regimurile de chimioterapie antitumorală de bază pentru gliomuri sunt considerate a fi:
- Lomustină 100 mg/m² în prima zi, vincristină 1,5 mg/m² în zilele 1 și opt, procarbazină 70 mg/m² din ziua opt până la douăzeci și primele, cursuri la fiecare șase săptămâni.
- Lomustină 110 mg/m² la fiecare șase săptămâni.
- Temozolomidă 5/23 150 până la 200 mg/m² din prima zi la a cincea, la fiecare 28 de zile.
- Temozolomidă ca parte a tratamentului de chimioradiere, 75 mg/m² în fiecare zi, se administrează radiații.
- Temozolomidă cu cisplatină sau carboplatină (80 mg/m²) și temozolomidă 150-200 mg/m² în zilele 1 până la 5 la fiecare 4 săptămâni.
- Temozolomidă 7/7 la 100 mg/m² în zilele 1-8 și 15-22 ale cursului, cu o repetare la fiecare patru săptămâni.
- Bevacizumab 5 până la 10 mg/kg în zilele 1 și cincisprezece, iar Irinotecan 200 mg/m² în zilele 1 și cincisprezece, s-au repetat la fiecare patru săptămâni.
- Bevacizumab 5 până la 10 mg/kg în zilele 1, cincisprezece și douăzeci și nouă, și Lomustina 90 mg/m² în prima zi la fiecare șase săptămâni.
- Bevacizumab 5 până la 10 mg/kg în zilele 1 și cincisprezece, lomustină 40 mg în zilele 1, opt, cincisprezece și douăzeci și două, repetate la fiecare șase săptămâni.
- Bevacizumab 5 până la 10 mg/kg în zilele 1 și cincisprezece, repetate la fiecare patru săptămâni.
În multe cazuri, medicamentele citostatice inhibă cu succes creșterea celulelor tumorale, dar nu arată selectivitate față de țesuturi și organe sănătoase. Prin urmare, experții au identificat o serie de contraindicații în care chimioterapia gliomului este imposibilă:
- Sensibilitate individuală excesivă la agenții chimiopreventivi;
- Decompensarea funcției cardiace, renale, hepatice;
- Hematopoieză deprimată în măduva osoasă;
- Probleme funcționale suprarenale.
Chimioterapia este administrată cu precauție extremă:
- Pacienți cu tulburări semnificative de ritm cardiac;
- Cu diabet;
- Pentru infecții virale acute;
- La pacienții vârstnici;
- Pacienții care suferă de alcoolism cronic (intoxicație cronică cu alcool).
Cel mai grav efect secundar al medicamentelor chimiopreventive este toxicitatea lor: citostaticii interferează selectiv cu funcționalitatea celulelor sanguine și își schimbă compoziția. În consecință, masa de trombocite și eritrocite scade și se dezvoltă anemia.
Înainte de a prescrie unui pacient un curs de chimioterapie, medicul ia întotdeauna în considerare gradul de toxicitate a medicamentelor și complicațiile probabile după utilizarea lor. Cursurile de chimioterapie sunt întotdeauna monitorizate cu atenție de către specialiști și monitorizarea regulată a sângelui.
Consecințele posibile ale terapiei citostatice:
- Gâdilare, emaciație;
- Dificultate înghițirea alimentelor, a mucoasei uscate, parodontită, dispepsie;
- Instabilitatea sistemului nervos central, tulburări maniacale-depresive, sindrom de convulsie, astenia;
- Deteriorarea funcției auditive;
- Creșterea tensiunii arteriale până la dezvoltarea crizei hipertensive;
- Scăderea trombocitelor, globulelor roșii, globulelor albe, hemoragii multiple, sângerări interne și externe;
- Insuficiență renală;
- Procese alergice;
- Căderea părului, aspectul zonelor de pigmentare crescută.
După cursuri de chimioterapie, pacienții au un risc crescut de a dezvolta boli infecțioase, iar durerea musculară și articulară este frecventă.
Pentru a reduce riscul de efecte adverse post-chemoterapeutice, sunt prescrise în mod necesar măsuri de reabilitare suplimentare, al cărui scop este restabilirea numărului normal de sânge, stabilizarea activității cardiovasculare, normalizarea stării neurologice. Se practică neapărat suficient sprijin psihologic suficient.
Tratament chirurgical
Intervenția chirurgicală este efectuată pentru a îndepărta cât mai mult posibil accentul tumorii, ceea ce la rândul său ar trebui să reducă presiunea intracraniană, să reducă insuficiența neurologică și să ofere biomaterialul necesar pentru cercetare.
- Chirurgia este efectuată într-un departament neurochirurgical specializat sau o clinică ale cărei specialiști sunt experimentați în intervenții neuro-oncologice.
- Chirurgul efectuează acces prin trepanarea oaselor din plastic în zona localizării gliomului suspectate.
- Dacă neoplasmul este localizat anatomic aproape de zonele motorii sau de căi, sau în nuclee sau de-a lungul nervilor cranieni, se utilizează monitorizarea neurofiziologică intraoperatorie.
- Sistemele de neuronavigare, navigarea fluorescentă intraoperatorie cu acid 5-aminolevulenic este de dorit să maximizeze îndepărtarea neoplasmului.
- După intervenție, în ziua 1-2 se efectuează un control CT sau RMN (cu sau fără injecție de contrast).
Dacă rezecția chirurgicală a gliomului este imposibilă sau recunoscută inițial ca inexpedient sau dacă se suspectează limfomul sistemului nervos central, se efectuează o biopsie (deschisă, stereotactică, cu monitorizare de navigație etc.). |
Pacienții cu gliomatoză cerebrală sunt verificați prin biopsie stereotactică, deoarece tactica terapeutică depind în mare măsură de imaginea histologică. |
În anumite situații - la pacienții vârstnici, în caz de tulburări neurologice severe, în cazul localizării gliomului în portbagaj și alte părți vitale - tratamentul este planificat pe baza simptomelor și informațiilor imagistice după o consultare medicală generală. |
Pacienții cu astrocitom piloid, precum și forme nodulare de neoplasme de trunchi și procese exofite sunt recomandate să fie supuse rezecției sau biopsiei deschise. |
Pacienții cu gliom pontin difuz și alte neoplasme difuze ale trunchiului sunt tratate cu radiații și terapie medicamentoasă antitumorală. Verificarea nu este necesară în astfel de cazuri. |
Pacienții cu gliom cu placă quadriplegică suferă rezonanță magnetică sistematică și monitorizare clinică după îndepărtarea hidrocelului cerebral. Dacă neoplasmul prezintă semne de creștere, acesta este îndepărtat cu o iradiere suplimentară. |
Atunci când se efectuează rezecția parțială sau biopsia unui gliom malign de grad scăzut, pacienții cu doi sau mai mulți factori de risc sunt tratați în mod necesar cu radiații și/sau chimioterapie. |
Rezecția totală este obligatorie pentru pacienții cu astrocitom cu celule gigant subependimale. |
Everolimus este prescris pentru astrocitomul celulelor gigant subpendente difuze. |
Astrocitomul piloid trebuie îndepărtat cu imagistica prin rezonanță magnetică după intervenție pentru a clarifica calitatea rezecției radicale a țesutului tumoral. |
În glioblastom, terapia postoperatorie trebuie combinată (radiații + chimioterapie) cu administrarea de temozolomidă. |
În astrocitomul anaplastic după operație, este indicată radioterapia cu terapie medicamentoasă suplimentară. Se folosesc lomustină, temozolomidă. |
Pacienții cu oligodendrogliom anaplastic sau oligoastrocitom primesc atât radiații, cât și chimioterapie (temozolomidă sau monoterapie PCV) după operație. |
Pacienții vârstnici cu gliom malign mare extins sunt iradiați în modul hipofracționat sau se efectuează monoterapie cu temozolomidă. |
În cazul recurenței gliomului, posibilitatea reoperării și a tacticii ulterioare de tratament sunt discutate de un consiliu de specialiști. Regimul optim pentru recurențe: reoperare + chimioterapie sistemică + expunere repetată la radiații + măsuri paliative. Dacă există zone minore localizate de creștere a tumorii recurente, se poate utiliza radiochirurgie. |
Medicamentele la alegere pentru creșterea recurentă a gliomului sunt temozolomida și bevacizumab. |
Reapariția oligodendrogliomelor extrem de maligne și a astrocitomelor anaplastice este o indicație pentru tratamentul cu temozolomidă. |
Xantoastrocitomul pleomorfic este îndepărtat fără chimioterapie adjuvantă obligatorie. |
Una dintre particularitățile gliomelor este dificultatea în tratamentul și îndepărtarea lor. Chirurgul își propune să îndepărteze țesuturile neoplasmului cât mai complet posibil, pentru a obține compensarea afecțiunii. Mulți pacienți sunt capabili să îmbunătățească calitatea vieții și să o prelungească, dar pentru tumori extrem de maligne, prognosticul rămâne nefavorabil: există o probabilitate crescută de re-creștere a focalizării patologice.
Nutriție pentru gliomul creierului
Dieta pentru pacienții cu tumori maligne - un punct important, care, din păcate, mulți oameni nu acordă prea multă atenție. Între timp, datorită schimbărilor în dietă, este posibil să încetinească dezvoltarea gliomului și să consolideze și să se agite imunitatea.
Zonele majore ale schimbărilor dietetice:
- Normalizarea proceselor metabolice, consolidarea protecției imunitare;
- Detoxifierea corpului;
- Optimizarea potențialului energetic;
- Asigurarea funcționării normale a tuturor organelor și sistemelor corpului într-o perioadă atât de dificilă pentru ele.
Dieta rațională și echilibrată este necesară, deoarece pacienții cu stadii timpurii de neoplasme maligne scăzute și pacienți cu ultima etapă de glioblastom. Dieta selectată cu atenție contribuie la îmbunătățirea bunăstării generale, a recuperării țesuturilor deteriorate, ceea ce este deosebit de important pe fondul tratamentului citostatic și de radiații. Echilibrul componentelor nutritive și procesele metabolice adecvate împiedică formarea de focare infecțioase, blochează reacțiile inflamatorii, previne epuizarea organismului.
Următoarele alimente și băuturi sunt recomandate pentru gliomul creierului:
- Fructe și legume colorate roșii, galbene și portocalii (roșii, piersici, caise, morcovi, sfeclă, fructe de citrice) care conțin carotenoizi, care protejează celulele sănătoase de efectele negative ale radioterapiei;
- Varză (conopidă, broccoli, varză de Bruxelles), ridiche, muștar și alte produse vegetale care conțin indol - o substanță activă care neutralizează factori adverși toxici și chimici;
- Verdeață (mărar, pătrunjel, tânără de păpădie și frunze de urzică, rubarbă, arugula, spanac), mazăre verde și sparanghel, fasole de sparanghel și alge (alge marine, spirulina, clorella);
- Ceai verde;
- Usturoi, ceapă, ananas, care au anti-tumoră și capacitate de detoxifiere;
- Bran, cereale, pâine cu cereale integrale, varză încolțită de leguminoase, cereale și semințe;
- Struguri întunecate, zmeură, căpșuni și căpșuni, afine, mure, rodie, coacăze, coacăze negre, rowanberries, afine, cătină de mare, cireșe și alte fructe de pădure care conțin antioxidanți naturali care reduc efectele negative ale radicalilor liberi, virusuri și carcasei;
- Produse lactate cu conținut scăzut de grăsimi.
Nu ar trebui să împovărați sistemul digestiv și întregul corp cu alimente grele și grase. Este util să folosiți sucuri de casă proaspăt stoarse, smoothie-uri, morcovi. Ar trebui adăugate surse de acizi grași omega-3, cum ar fi uleiul de pește, uleiul de semințe de in sau semințele de in.
Este mai bine să evitați zahărul și dulciurile cu totul. Dar o lingură de miere cu o cană de apă nu va face rău: produsele de albine au un efect antiinflamator, antioxidant și antitumoral pronunțat. Singura contraindicație la utilizarea mierii este o alergie la produs.
Din dietă ar trebui exclusă:
- Carne, untură, offal;
- Unt, produse lactate grase;
- Carne afumată, cârnați, carne de conserve și pește;
- Alcool sub orice formă;
- Dulciuri, produse de patiserie, prăjituri și produse de patiserie, bomboane și bomboane de ciocolată;
- Alimente convenabile, fast-food, gustări;
- Alimente prăjite.
Ar trebui să consumi suficiente legume, verzi, fructe și apă potabilă curată zilnic.
În timpul chimioterapiei și pentru ceva timp după ea, ar trebui să bei sucuri de legume și fructe de casă, să mănânci brânză de casă cu conținut scăzut de grăsimi, lapte și brânză. Este important să beți multe lichide, să vă spălați dinții și să vă clătiți des gura (de aproximativ 4 ori pe zi).
Mese optime pentru pacienții cu gliom cerebral:
- Caserole vegetale;
- Feluri de mâncare laterale și supe din cereale (de preferință hrișcă, ovăz, orez, cuscus, bulgur);
- Cheesecakes cu aburi, budinci, caserole;
- Legume fundașate și coapte;
- Tocanite, supe de legume, primul și al doilea feluri de mâncare din leguminoase (inclusiv soia), pates și soufflés;
- Smoothie-uri, ceai verde, compote și morcovi.
Profilaxie
Dacă o persoană conduce un stil de viață sănătos, iar printre rudele sale nu au existat cazuri de patologie a cancerului, el are toate șansele să nu obțină gliomul creierului. Nu există o prevenire specifică a unor astfel de tumori, astfel încât principalele puncte de prevenire sunt considerate a fi o nutriție adecvată, activitate fizică, evitarea obiceiurilor proaste, absența pericolelor profesionale și gospodărești.
Specialiștii oferă o serie de recomandări simple, dar eficiente:
- Bea mai multă apă pură, evită sodă îndulcită, sucuri ambalate, băuturi energizante și alcool.
- Evitați pericolele profesionale și gospodărești: mai puțin contact cu substanțele chimice, soluții corozive și lichide.
- Încercați să pregătiți mâncare prin fierbere, tocanire, coacere, dar nu prăjiți. Oferiți preferință pentru alimentele de casă sănătoase, de calitate.
- O mare parte din dieta dvs. ar trebui să fie alimentele vegetale, inclusiv verdeața, indiferent de perioada anului.
- Un alt factor negativ este să fie supraponderal, care ar trebui să fie scăzut. Controlul greutății este foarte important pentru sănătatea întregului corp.
- Uleiurile vegetale ar trebui să fie întotdeauna preferate peste unt și untură.
- Dacă este posibil, este de dorit să acordăm preferință produselor ecologice, carne fără hormoni, legume și fructe fără nitrați și pesticide. Este mai bine să evitați carnea roșie cu totul.
- Nu luați preparate multivitamine fără indicații și în cantități mari. Nu luați niciun medicament fără prescripția medicului: auto-medicația este adesea foarte, foarte periculoasă.
- Dacă apar simptome suspecte, este necesar să vizitați un medic, fără a aștepta agravarea situației, dezvoltarea efectelor și complicațiilor adverse.
- Dulciurile și alimentele cu un indice glicemic ridicat sunt o componentă nedorită a dietei.
- Cu cât o persoană mai anterioară se duce la medici, cu atât șansele sale de vindecare sunt mai mari (și acest lucru se aplică aproape oricărei boli, inclusiv gliomului creierului).
Pentru a preveni formarea oncopatologiei, aveți nevoie de suficient timp pentru a dormi și a vă odihni, evitați consumul excesiv de băuturi alcoolice, dați preferință pentru alimentele naturale de înaltă calitate, reduceți utilizarea gadgeturilor (în special, telefoanele mobile).
Bolile tumorale apar adesea la vârstnici și la bătrâni. Prin urmare, este important să vă monitorizați propria sănătate de la o vârstă fragedă și să nu provocați procese patologice prin stilul de viață nesănătos și obiceiurile nesănătoase.
Cauzele principale exacte ale oncologiei nu au fost încă clarificate. Cu toate acestea, un anumit rol, desigur, joacă condiții profesionale și de mediu nefavorabile, expunerea la radiații ionizante și electromagnetice, modificări hormonale. Nu rămâneți mult timp și în mod regulat sub soare, lăsați schimbări bruște ale temperaturii ambientale, supraîncălziți în baie sau saună, adesea luați băi calde sau dușuri.
O altă întrebare: cum să prevină reapariția gliomului cerebral după tratamentul său de succes? Reapariția creșterii neoplasmei este o complicație complexă și, din păcate, frecventă, care este dificil de prezis în avans. Pacienții li se poate recomanda să facă examene și verificări preventive periodice, să viziteze un oncolog și să participe la medicul cel puțin de două ori pe an, să conducă un stil de viață sănătos, să mănânce alimente sănătoase și naturale, să practice o activitate fizică moderată. O altă afecțiune este dragostea de viață, optimismul sănătos, atitudinea pozitivă față de succes în orice circumstanțe. Aceasta include, de asemenea, o atmosferă prietenoasă în familie și la serviciu, răbdare și sprijin necondiționat din partea oamenilor apropiați.
Prognoză
Starea creierului și caracteristicile gliomului la momentul detectării sale influențează rata de supraviețuire la fel de mult ca tratamentul administrat. O sănătate generală satisfăcătoare a pacientului și vârsta sa îmbunătățește prognosticul (prognosticul este mai optimist la pacienții tineri). Un indicator important este imaginea histologică a neoplasmului. Astfel, gliomele de grad scăzut au un prognostic mai bun decât gliomele anaplastice și, cu atât mai mult, glioblastoame (cele mai nefavorabile procese tumorale). Astrocitomele au un prognostic mai rău decât oligodendrogliomele.
Astrocitomele maligne răspund slab la terapie și au o rată de supraviețuire relativ mică de șase până la cinci ani. În același timp, speranța de viață în gliomele de grad scăzut este estimată la 1-10 ani.
Astrocitomele maligne sunt în esență incurabile. Direcția de tratament implică de obicei reducerea manifestărilor neurologice (inclusiv disfuncția cognitivă) și creșterea speranței de viață, menținând în același timp cea mai înaltă calitate a vieții. Terapia simptomatică este atrasă pe fondul măsurilor de reabilitare. Munca unui psiholog este, de asemenea, importantă.
În ultimul deceniu, oamenii de știință au făcut unele progrese în înțelegerea naturii tumorilor cerebrale și a modului de a le trata. Ar trebui să se facă mult mai multe pentru a optimiza prognosticul bolii. Sarcina principală a specialiștilor astăzi este următoarea: gliomul creierului ar trebui să aibă mai multe scheme pentru eliminarea eficientă a problemei simultan, atât în etapele timpurii, cât și cele ulterioare ale dezvoltării.

