Noile publicații
Cum „mușcă” un embrion din țesutul matern: mecanica implantării la oameni, filmată în timp real pentru prima dată
Ultima examinare: 23.08.2025

Tot conținutul iLive este revizuit din punct de vedere medical sau verificat pentru a vă asigura cât mai multă precizie de fapt.
Avem linii directoare de aprovizionare stricte și legătura numai cu site-uri cu reputație media, instituții de cercetare academică și, ori de câte ori este posibil, studii medicale revizuite de experți. Rețineți că numerele din paranteze ([1], [2], etc.) sunt link-uri clickabile la aceste studii.
Dacă considerați că oricare dintre conținuturile noastre este inexactă, depășită sau îndoielnică, selectați-o și apăsați pe Ctrl + Enter.
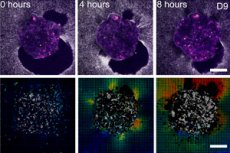
Oamenii de știință de la Barcelona (IBEC, Dexeus Mujer) și Tel Aviv au demonstrat pentru prima dată în timp real și în 3D cum un embrion uman se atașează de „schela uterină” și, la propriu, trage și restructurează țesutul înconjurător. Pentru a realiza acest lucru, au creat o platformă ex vivo deformabilă (geluri de colagen/ECM) și au aplicat microscopia cu forță de tracțiune direct pe embrioni umani și de șoarece vii. Principala constatare: modelul forțelor este specific speciei, iar embrionii înșiși sunt mecanosensibili: aceștia răspund la semnale mecanice externe prin restructurarea citoscheletului și schimbarea orientării creșterii.
Contextul studiului
Implantarea este „blocajul” reproducerii umane: în această etapă, atât concepțiile naturale, cât și încercările de fertilizare in vitro (FIV) eșuează cel mai adesea. În același timp, implantarea umană este interstițială: embrionul nu se „lipește” pur și simplu, ci este complet încorporat în endometru - un proces complex din punct de vedere biochimic și mecanic, dar până de curând aproape neobservat în sistemele vii la om. Prin urmare, mecanica aderenței și invaziei a rămas o „cutie neagră”, iar concluziile au fost adesea trase pe baza unor markeri indirecți sau a datelor provenite de la modele animale.
Biologia clasică a implantării s-a bazat în mare măsură pe șoareci, dar există diferențe fundamentale între specii, de la orientarea blastocistului la adâncimea implantării și modelul forțelor celulare. La șoareci, implantarea este mai „superficială”, cu direcții preferențiale de deplasare a țesuturilor; la oameni, este distinct invazivă, cu forțe de tracțiune multifocale în jurul embrionului. Aceste diferențe sugerează că modelul de șoarece nu se potrivește întotdeauna cu cel uman, mai ales când vine vorba de mecanică. Au fost necesare observații directe ale embrionului uman într-un mediu deformabil.
Descoperirea tehnologică a fost posibilă prin combinarea matricilor 2D/3D deformabile (colagen/ECM) și a microscopiei cu forță de tracțiune cu imagistica de înaltă frecvență pe termen lung. Acest „uter artificial” a făcut posibilă observarea și măsurarea modului în care embrionul trage, restructurează și „găurește” țesutul înconjurător – și cum răspunde la semnale mecanice externe (mecanosensibilitate). Aceasta deschide calea către noi criterii pentru evaluarea potențialului de implantare și pentru reglarea fină a condițiilor de transfer de embrioni.
Contextul este aplicat: dacă proprietățile mecanice ale mediului și modelul forțelor embrionare sunt asociate cu succesul implantării, atunci în FIV este posibil să se selecteze în mod intenționat rigiditatea/compoziția matricei, să se țină cont de ferestrele de timp ale transferului și chiar să se utilizeze metrici de „forță” ca marker suplimentar de selecție. În paralel, astfel de platforme vor ajuta la explicarea proporției pierderilor de sarcină timpurii, atunci când biochimia este „normală”, dar mecanica aderenței nu este. Toate acestea fac ca observațiile 3D directe ale implantării umane să nu fie doar un videoclip frumos, ci un nou instrument pentru medicina reproductivă.
De ce este important acest lucru?
Eșecul implantării este una dintre principalele cauze ale infertilității și reprezintă până la 60% din cazurile de avorturi spontane. În ciuda progreselor biochimice în fertilizarea in vitro, mecanismele acestui proces la om au rămas o „cutie neagră”. O nouă abordare ne permite să vedem forțele și traiectoriile implantării embrionilor și oferă o bază pentru îmbunătățirea condițiilor de selecție și transfer a embrionilor.
Cum s-a făcut
Cercetătorii au asamblat un „uter artificial” - un mediu moale, transparent și deformabil în care o matrice asemănătoare țesutului se mișcă vizibil sub influența forțelor embrionare. Apoi au urmat microscopia continuă și analiza computațională a deplasărilor fibrelor.
- Platforme 2D și 3D: în 3D, embrionul este imediat încorporat în matrice (stadiul de atașare este „ocolit”), ceea ce permite observarea găuririi în grosimea țesutului.
- „Supraviețuire și penetrare” ridicată în 3D: aproximativ 80% invazie reușită (limitată de proximitatea sticlei).
- Hărțile de tracțiune și corelația digitală a volumului arată amplitudinile și direcțiile deplasărilor în jurul embrionului - în esență o „amprentă” a forței în timp.
Ce s-a constatat exact (pe scurt și punct cu punct)
1) Mecanica implantării specifice speciei
- Om: embrionul este inserat în matrice, creând multiple focare de tracțiune și formând deplasări radial uniforme în jurul său; adâncimea invaziei este de până la 200 µm.
- Șoarece: embrionul se răspândește în principal pe suprafață, cu direcții principale de deplasare pronunțate.
2) Embrionul simte mecanismele mediului înconjurător
- Forțe externe → răspuns: la embrionul uman - recrutarea miozinei și a pseudopodiilor celulare direcționate; la șoarece - rotația axei de implantare/creștere către sursa forței externe (orientarea axei PD).
- Markeri mecanosensibili: la șoarece, modificări ale localizării YAP în trofoblast; împreună, acestea indică un circuit de feedback mecanosensibil.
3) Relația dintre rezistență și succesul implantării
- Deplasare mai mică a colagenului → progres mai slab al implantării la embrionii umani.
- Integrine - „cuplatorul” de putere: blocarea peptidelor RGD/inhibarea Src la șoareci reduce adâncimea/aria de implantare.
Cum arată implementarea?
- Pe platformele 2D și 3D, în jurul embrionului se formează un „halou” crescător de fibre care se deplasează în jurul lor; harta de tracțiune pulsează ca și cum embrionul și-ar „scana” împrejurimile.
- Pe sticlă, embrionul uman formează o excrescență plată, dar într-o matrice moale rămâne mai sferic și merge mai adânc - ca în țesutul viu.
Ce oferă acest lucru practicii (perspective pentru FIV și nu numai)
Ideea este simplă: implantarea nu este doar „chimia receptorilor”, ci și mecanica aderenței și tracțiunii. Aceasta înseamnă că putem optimiza:
- Duritatea materialelor și a mediului în timpul testelor de potențial de cultură/implantare;
- Noi markeri pentru selecția embrionilor - bazați pe traiectorii și amplitudinea deplasărilor în matricea „inteligentă”;
- Antrenament/modulare uterină (de exemplu, prin indicii mecanice blânde) pentru îmbunătățirea aderenței fără intervenții agresive.
Atenție: munca ex vivo nu se desfășoară „în interiorul uterului”. Însă însuși faptul că un semnal mecanic extern modifică orientarea implantării/organizării axelor deschide calea către condiții personalizate de transfer de embrioni.
Restricții
- Modelul ex vivo nu ia în considerare dinamica imună, hormonală și vasculară a endometrului real;
- Matrigelul/colagenul definesc un set de proprietăți (rigiditate, viscoelasticitate, compoziție), fiind dificil să le modifici cu un singur parametru;
- Constrângerile etice pentru studiile pe oameni (fereastră de până la 14 zile) limitează observațiile pe termen lung. Cu toate acestea, concordanța ridicată cu modurile de implantare in vivo cunoscute (interstițială la oameni vs. superficială la șoareci) crește încrederea în model.
Concluzie
Embrionul uman își „trage” și „forează” în mod activ țesutul matern, iar indiciile mecanice din mediu îi pot reconfigura comportamentul. Modelul forțelor și strategia de implantare sunt diferite la oameni și șoareci - iar acest lucru ar putea explica de ce modelul șoarece nu prezice întotdeauna implantarea cu succes la oameni. Mecanica este acum un actor cu drepturi depline în embriologia timpurie și medicina reproductivă.
Sursa: Godeau AL și colab. Forța de tracțiune și mecanosensibilitatea mediază modelele de implantare specifice speciei în embrionii umani și de șoarece. Science Advances 11(33): eadr5199 (15 august 2025). DOI: 10.1126/sciadv.adr519
