Noile publicații
Sistemul de livrare a medicamentelor cu circuit închis ar putea îmbunătăți chimioterapia
Ultima examinare: 14.06.2024

Tot conținutul iLive este revizuit din punct de vedere medical sau verificat pentru a vă asigura cât mai multă precizie de fapt.
Avem linii directoare de aprovizionare stricte și legătura numai cu site-uri cu reputație media, instituții de cercetare academică și, ori de câte ori este posibil, studii medicale revizuite de experți. Rețineți că numerele din paranteze ([1], [2], etc.) sunt link-uri clickabile la aceste studii.
Dacă considerați că oricare dintre conținuturile noastre este inexactă, depășită sau îndoielnică, selectați-o și apăsați pe Ctrl + Enter.
Când pacienții cu cancer sunt supuși chimioterapiei, dozele majorității medicamentelor sunt calculate pe baza suprafeței corporale a pacientului. Acest indicator este estimat folosind o ecuație în care sunt înlocuite înălțimea și greutatea pacientului. Această ecuație a fost formulată în 1916 pe baza datelor de la doar nouă pacienți.
Această abordare simplistă a dozării nu ține cont de alți factori și poate duce la prescrierea pacientului prea mult sau prea puțin din medicament. Drept urmare, unii pacienți pot prezenta toxicitate excesivă sau lipsă de eficacitate a chimioterapia.
Pentru a îmbunătăți acuratețea dozării chimioterapiei, inginerii MIT au dezvoltat o abordare alternativă care permite ca doza să fie personalizată pentru fiecare pacient. Sistemul lor măsoară cantitatea de medicament din corpul pacientului, iar aceste date sunt introduse în controler, care poate ajusta rata de perfuzie în consecință.
Această abordare poate ajuta la compensarea diferențelor în farmacocinetica medicamentului cauzate de compoziția corpului, predispoziția genetică, toxicitatea organului indusă de chimioterapie, interacțiunile cu alte medicamente și alimente și fluctuațiile circadiene ale enzimelor responsabile de descompunerea medicamentelor pentru chimioterapie, spun cercetătorii. p>
„Prin recunoașterea progreselor în înțelegerea modului în care medicamentele sunt metabolizate și prin aplicarea instrumentelor de inginerie pentru a simplifica dozarea personalizată, credem că putem contribui la transformarea siguranței și eficacității multor medicamente”, spune Giovanni Traverso, profesor asistent de inginerie mecanică la MIT și un gastroenterolog la spital. Brigham and Women's Hospital și autor principal al studiului.
Louis DeRidder, un student absolvent al MIT, este autorul principal al lucrării publicate în Med.
Monitorizare continuă
În acest studiu, cercetătorii s-au concentrat pe un medicament numit 5-fluorouracil, care este utilizat pentru a trata cancerul colorectal și alte tipuri de cancer. Medicamentul este de obicei administrat pe o perioadă de 46 de ore, iar doza este determinată folosind o formulă bazată pe înălțimea și greutatea pacientului, care oferă o estimare a suprafeței corporale.
Cu toate acestea, această abordare nu ține cont de diferențele de compoziție corporală, care pot afecta distribuția medicamentului în organism, sau de variațiile genetice care îi afectează metabolismul. Aceste diferențe pot duce la efecte secundare dăunătoare dacă există prea mult medicament. Dacă medicamentul nu este suficient, este posibil să nu omoare tumora așa cum era de așteptat.
„Oamenii cu aceeași suprafață corporală pot avea înălțimi și greutăți foarte diferite, masă musculară sau genetică diferită, dar atâta timp cât înălțimea și greutatea introduse în această ecuație oferă aceeași suprafață corporală, doza lor este identică.” spune DeRidder, un candidat la doctorat în programul de inginerie medicală și fizică medicală din cadrul programului de științe și tehnologie a sănătății Harvard-MIT.
Un alt factor care poate modifica cantitatea de medicament din sânge la un moment dat este fluctuația circadiană a unei enzime numită dihidropirimidin dehidrogenază (DPD), care descompune 5-fluorouracilul. Expresia DPD, ca multe alte enzime din organism, este reglată de un ritm circadian. Astfel, degradarea 5-FU DPD nu este constantă, ci variază în funcție de momentul zilei. Aceste ritmuri circadiene pot duce la fluctuații de zece ori ale cantității de 5-fluorouracil din sângele unui pacient pe parcursul unei perfuzii.
„Folosind suprafața corpului pentru a calcula doza de chimioterapie, știm că doi oameni pot avea toxicități complet diferite față de 5-fluorouracil. Un pacient poate avea cicluri de tratament cu toxicitate minimă și apoi un ciclu cu toxicitate teribilă. Ceva s-a schimbat în modul în care acest lucru pacientul a metabolizat chimioterapia de la un ciclu la altul Metoda noastră de dozare învechită nu surprinde aceste modificări, iar pacienții suferă ca urmare”, spune Douglas Rubinson, medic oncolog la Dana-Farber Cancer Institute și autorul lucrării.
O modalitate de a încerca să compenseze variabilitatea farmacocineticii chimioterapiei este o strategie numită monitorizare terapeutică a medicamentelor, în care pacientul furnizează o probă de sânge la sfârșitul unui ciclu de tratament. După ce această probă este analizată pentru concentrațiile medicamentului, doza poate fi ajustată, dacă este necesar, la începutul următorului ciclu (de obicei, după două săptămâni pentru 5-fluorouracil).
S-a demonstrat că această abordare conduce la rezultate mai bune pentru pacienți, dar nu a fost utilizată pe scară largă pentru chimioterapii, cum ar fi 5-fluorouracil.
Cercetătorii MIT au dorit să dezvolte un tip similar de monitorizare, dar într-un mod automat, care ar putea personaliza doza de medicament în timp real, ceea ce ar putea duce la rezultate mai bune pentru pacienți.
În sistemul lor în buclă închisă, concentrațiile medicamentului pot fi monitorizate continuu, iar aceste informații sunt utilizate pentru a ajusta automat rata de perfuzie a medicamentului pentru chimioterapie pentru a menține doza în intervalul țintă.
Acest sistem în buclă închisă permite personalizarea dozării medicamentului pentru a ține cont de ritmurile circadiene ale nivelurilor în schimbare ale enzimelor de metabolizare a medicamentelor, precum și de orice modificări ale farmacocineticii pacientului de la ultimul tratament, cum ar fi toxicitatea de organ indusă de chimioterapie.
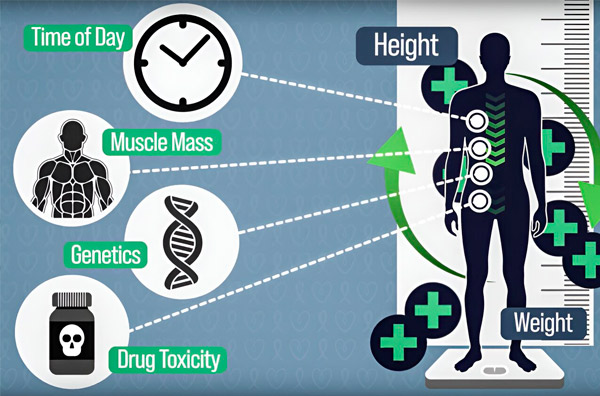
Pentru a face dozarea chimioterapiei mai precisă, inginerii MIT au dezvoltat o modalitate de a măsura continuu cantitatea de medicament din corpul unui pacient în timpul unei perfuzii de ore. Acest lucru va ajuta la compensarea diferențelor cauzate de compoziția corpului, genetică, toxicitatea medicamentelor și fluctuațiile circadiene. Sursa: furnizată de cercetători.
Noul sistem dezvoltat de cercetători, cunoscut sub numele de CLAUDIA (Closed-Loop AUtomated Drug Infusion regulator), utilizează echipamente disponibile în comerț pentru fiecare pas. Se prelevează probe de sânge la fiecare cinci minute și se prepară rapid pentru analiză. Concentrația de 5-fluorouracil din sânge este măsurată și comparată cu intervalul țintă.
Diferența dintre concentrațiile țintă și măsurate este introdusă în algoritmul de control, care ajustează apoi viteza de perfuzie, dacă este necesar, pentru a menține doza în intervalul de concentrație la care medicamentul este eficient și non-toxic.
„Am dezvoltat un sistem în care putem măsura continuu concentrațiile de medicamente și putem ajusta rata de perfuzie în consecință pentru a menține concentrațiile medicamentului în fereastra terapeutică”, spune DeRidder.
Ajustare rapidă
În testele pe animale, cercetătorii au descoperit că, folosind CLAUDIA, au reușit să mențină cantitatea de medicament care circulă în organism în intervalul țintă de aproximativ 45% din timp.
Nivelurile de medicamente la animalele care au primit chimioterapie fără CLAUDIA au rămas în intervalul țintă doar 13% din timp, în medie. În acest studiu, cercetătorii nu au testat eficacitatea nivelurilor de medicamente, dar se crede că menținerea concentrațiilor în fereastra țintă duce la rezultate mai bune și o toxicitate mai mică.
CLAUDIA a reușit, de asemenea, să mențină doza de 5-fluorouracil în intervalul țintă chiar și atunci când i-a fost administrat un medicament care inhibă enzima DPD. La animalele tratate cu acest inhibitor fără monitorizare și ajustare continuă, nivelurile de 5-fluorouracil au crescut de până la opt ori.
Pentru această demonstrație, cercetătorii au efectuat manual fiecare pas al procesului folosind echipamente disponibile, dar acum intenționează să automatizeze fiecare pas, astfel încât monitorizarea și ajustările dozei să se poată face fără intervenția umană.
Pentru a măsura concentrațiile de medicamente, cercetătorii au folosit cromatografie lichidă de înaltă performanță-spectrometrie de masă (HPLC-MS), o tehnică care poate fi adaptată pentru a detecta practic orice tip de medicament.
„Ne imaginăm un viitor în care putem folosi CLAUDIA pentru orice medicament care are proprietăți farmacocinetice adecvate și care este detectabil prin HPLC-MS, permițând dozarea personalizată pentru multe medicamente diferite”, spune DeRidder.
