Noile publicații
Studiul relevă interacțiunile dintre proteine ca potențială cale de vindecare a sclerozei amiotrofice laterale
Ultima examinare: 02.07.2025

Tot conținutul iLive este revizuit din punct de vedere medical sau verificat pentru a vă asigura cât mai multă precizie de fapt.
Avem linii directoare de aprovizionare stricte și legătura numai cu site-uri cu reputație media, instituții de cercetare academică și, ori de câte ori este posibil, studii medicale revizuite de experți. Rețineți că numerele din paranteze ([1], [2], etc.) sunt link-uri clickabile la aceste studii.
Dacă considerați că oricare dintre conținuturile noastre este inexactă, depășită sau îndoielnică, selectați-o și apăsați pe Ctrl + Enter.

În Canada, datorită filantropiei, o echipă de cercetători de la Universitatea Western Ontario, condusă de Dr. Michael Strong, a descoperit un potențial leac pentru scleroza laterală amiotrofică (SLA).
Studiul, care ilustrează modul în care interacțiunile dintre proteine pot păstra sau preveni moartea celulelor nervoase, caracteristică SLA, este punctul culminant al deceniilor de cercetare susținute de Fundația Temerty.
„Ca medic, este foarte important pentru mine să pot spune unui pacient sau unei familii: «Încercăm să oprim această boală»”, a spus Strong, un clinician-cercetător care și-a dedicat cariera găsirii unui leac pentru SLA. „Ne-au trebuit 30 de ani de muncă pentru a ajunge aici; 30 de ani de îngrijire a familiilor, pacienților și a celor dragi lor, când tot ce aveam era speranța. Asta ne dă motive să credem că am găsit un leac.”
SLA, cunoscută și sub numele de boala Lou Gehrig, este o tulburare neurodegenerativă debilitantă care perturbă progresiv celulele nervoase responsabile de controlul muscular, ducând la atrofie musculară, paralizie și, în cele din urmă, moarte. Speranța medie de viață pentru un pacient cu SLA după diagnosticare este de numai doi până la cinci ani.
Într-un studiu publicat în revista Brain, echipa lui Strong a descoperit că țintirea interacțiunii dintre două proteine prezente în celulele nervoase afectate de SLA poate opri sau inversa progresia bolii. Echipa a identificat, de asemenea, mecanismul care face acest lucru posibil.
„Este important de menționat că această interacțiune poate fi esențială pentru dezvoltarea de tratamente nu doar pentru SLA, ci și pentru alte afecțiuni neurologice conexe, cum ar fi demența frontotemporală”, a declarat Strong, care deține catedra Arthur J. Hudson în cercetarea SLA la Școala de Medicină și Stomatologie Schulich a Universității Western. „Aceasta este o schimbare radicală.”
La aproape toți pacienții cu SLA, o proteină numită TDP-43 este responsabilă de formarea unor aglomerări anormale în interiorul celulelor, provocând moartea acestora. În ultimii ani, echipa lui Strong a descoperit o a doua proteină, numită RGNEF, care funcționează în opoziție cu TDP-43.
Cea mai recentă descoperire a echipei a identificat un fragment specific al acestei proteine RGNEF, numit NF242, care poate atenua efectele toxice ale proteinei care cauzează SLA. Cercetătorii au descoperit că, atunci când cele două proteine interacționează una cu cealaltă, toxicitatea proteinei care cauzează SLA este eliminată, reducând semnificativ deteriorarea celulelor nervoase și prevenind moartea acestora.
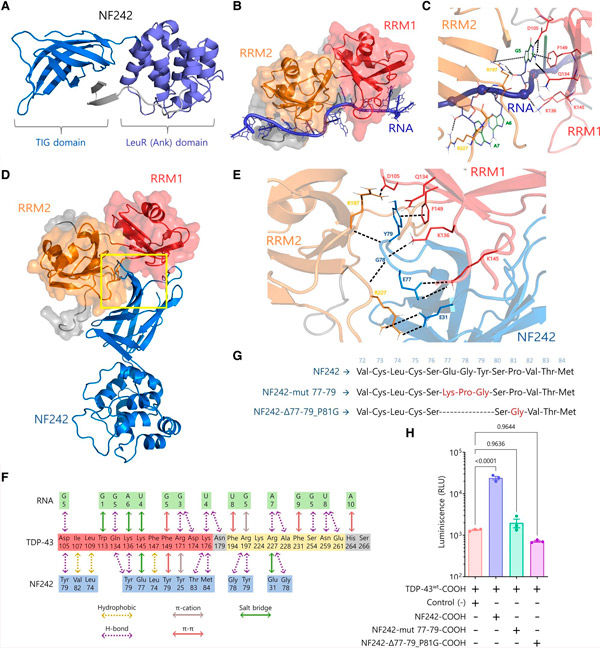
Modelarea interacțiunii TDP-43-NF242. Sursa: Brain (2024). DOI: 10.1093/brain/awae078
În experimentele efectuate pe musculițe de fructe, această abordare a crescut semnificativ durata de viață, a îmbunătățit funcția motorie și a protejat celulele nervoase de degenerare. În mod similar, în modelele cu șoareci, abordarea a dus la creșterea duratei de viață și a mobilității, precum și la reducerea markerilor neuroinflamației.
Calea către descoperirea echipei a fost deschisă de investiția pe termen lung a familiei Temerty în cercetarea SLA la Universitatea Western – un sprijin pe care Strong îl numește „cu adevărat transformator”.
Acum, Strong și echipa sa și-au stabilit obiectivul de a aduce potențialul lor tratament în studii clinice pe oameni în termen de cinci ani, grație unei noi donații din partea Fundației Temerty.
Fondul, fondat de James Temerty, fondatorul Northland Power Inc., și Louise Arcand Temerty, investește 10 milioane de dolari pe parcursul a cinci ani pentru a sprijini următorii pași în aducerea acestui tratament pacienților cu SLA.

Dr. Michael Strong, deținătorul Catedrei Arthur J. Hudson în Cercetare SLA la Facultatea de Medicină și Stomatologie Schulich din cadrul Universității Western, a descoperit o proteină care ar putea duce la un leac pentru SLA. Credit: Allan Lewis / Facultatea de Medicină și Stomatologie Schulich
„Găsirea unui tratament eficient pentru SLA ar însemna enorm pentru persoanele care trăiesc cu această boală teribilă și pentru cei dragi lor”, a declarat James Temerty. „Universitatea Western împinge limitele cunoașterii despre SLA și suntem încântați să contribuim la următoarea fază a acestei cercetări inovatoare.”
Noua donație a Fundației Temerty aduce investiția totală a familiei în cercetarea bolilor neurodegenerative la Universitatea Western la 18 milioane de dolari.
„Dedicația neobosită a Dr. Strong față de cauza sa este egalată de dorința profundă a familiei Temerty de a face o diferență pentru miile de oameni din întreaga lume care au fost diagnosticați cu această boală devastatoare”, a declarat președintele Universității Western, Alan Shepard. „Investițiile și viziunea Fundației Temerty au accelerat progresul în găsirea unui tratament eficient pentru SLA. Suntem recunoscători pentru angajamentul familiei Temerty față de cercetarea care schimbă vieți.”
„Acesta este un moment de cotitură în cercetarea SLA care are potențialul de a schimba cu adevărat viața pacienților”, a declarat Dr. John Yu, decanul Facultății de Medicină și Stomatologie Schulich.
„Datorită conducerii Dr. Strong, investițiilor noastre continue în cele mai bune instrumente și tehnologii și sprijinului Fundației Temerty, suntem încântați să anunțăm o nouă eră a speranței pentru pacienții cu SLA.”
Rezultatele lucrării sunt descrise în detaliu într-un articol publicat în revista Brain.
