Noile publicații
Noile descoperiri contribuie la o mai bună înțelegere a cauzelor sindromului Rett
Ultima examinare: 02.07.2025

Tot conținutul iLive este revizuit din punct de vedere medical sau verificat pentru a vă asigura cât mai multă precizie de fapt.
Avem linii directoare de aprovizionare stricte și legătura numai cu site-uri cu reputație media, instituții de cercetare academică și, ori de câte ori este posibil, studii medicale revizuite de experți. Rețineți că numerele din paranteze ([1], [2], etc.) sunt link-uri clickabile la aceste studii.
Dacă considerați că oricare dintre conținuturile noastre este inexactă, depășită sau îndoielnică, selectați-o și apăsați pe Ctrl + Enter.

Sindromul Rett este o tulburare neurodezvoltării rară pentru care în prezent nu există leac sau tratament eficient. Acesta provoacă simptome fizice și cognitive severe, multe dintre ele suprapunându-se cu tulburările din spectrul autist.
Sindromul Rett este cauzat de mutații ale genei MECP2, care este puternic exprimată în creier și pare să joace un rol important în menținerea sănătății neuronilor. Gena este situată pe cromozomul X, iar sindromul afectează în principal fetele. Pentru a dezvolta tratamente pentru sindromul Rett, cercetătorii doresc să înțeleagă mai bine MECP2 și funcțiile sale în creier.
Cercetătorii, inclusiv cofondatorul Institutului Whitehead, Rudolf Jaenisch, studiază MECP2 de zeci de ani, însă multe aspecte de bază despre această genă au rămas necunoscute. Proteina codificată de genă, MECP2, este implicată în reglarea genelor; se leagă de ADN și influențează nivelurile de expresie ale altor gene sau cantitatea de proteine pe care o produc.
Cu toate acestea, cercetătorii nu aveau o listă completă a genelor afectate de MECP2 și nu exista un consens cu privire la modul în care MECP2 afectează aceste gene.
Studiile timpurii asupra MECP2 au sugerat că aceasta este un represor, reducând expresia genelor sale țintă, dar cercetările efectuate de Jaenisch și alții au arătat anterior că MECP2 acționează și ca un activator, crescând expresia genelor sale țintă - și că ar putea fi un activator în primul rând. De asemenea, nu se știa mecanismul de acțiune al MECP2 sau ce face exact proteina pentru a provoca modificări în expresia genelor.
Limitările tehnologice i-au împiedicat pe cercetători să obțină clarificări cu privire la aceste întrebări. Însă Yanish, Yi Liu, postdoctorand în laboratorul său, și Anthony Flamier, fost membru al laboratorului lui Yanish, acum profesor asistent la centrul de cercetare CHU Sainte-Justine din cadrul Universității din Montréal, au folosit tehnici de ultimă generație pentru a răspunde la aceste întrebări rămase despre MECP2 și pentru a obține noi perspective asupra rolului său în sănătatea și bolile creierului.
Rezultatele lor au fost publicate în revista Neuron, iar cercetătorii au creat și un depozit online al datelor lor MECP2, portalul MECP2-NeuroAtlas, ca resursă pentru alți cercetători.
„Cred că această lucrare va schimba fundamental înțelegerea oamenilor despre modul în care MECP2 provoacă sindromul Rett. Avem o înțelegere complet nouă a mecanismului și ar putea oferi noi căi pentru dezvoltarea de tratamente pentru această boală”, spune Janisch, care este și profesor de biologie la MIT.
Înțelegere mai profundă a MECP2 în creier
Cercetătorii au creat mai întâi o hartă detaliată a locului în care MECP2 se leagă în secvențele genelor neuronale umane, fie în cadrul genelor, fie în regiunile reglatoare ale ADN-ului din apropierea acestora. Au folosit o abordare numită CUT&Tag, care poate identifica cu precizie interacțiunile proteinelor cu ADN-ul.
Cercetătorii au descoperit peste 4.000 de gene asociate cu MECP2. Au repetat cartografierea în neuronii cu mutații MECP2 comune asociate cu sindromul Rett pentru a determina unde este epuizat MECP2 în starea de boală.
Cunoașterea genelor de care se leagă MECP2 le-a permis lui Liu și Flamier să înceapă să facă conexiuni între țintele MECP2 și sănătatea creierului. Ei au descoperit că multe dintre țintele sale sunt implicate în dezvoltarea și funcționarea axonilor și sinapselor neuronale.
De asemenea, au comparat lista lor de ținte MECP2 cu baza de date a Inițiativei de Cercetare a Autismului a Fundației Simons (SFARI) privind genele asociate cu autismul și au descoperit că 381 de gene din acea bază de date sunt ținte MECP2.
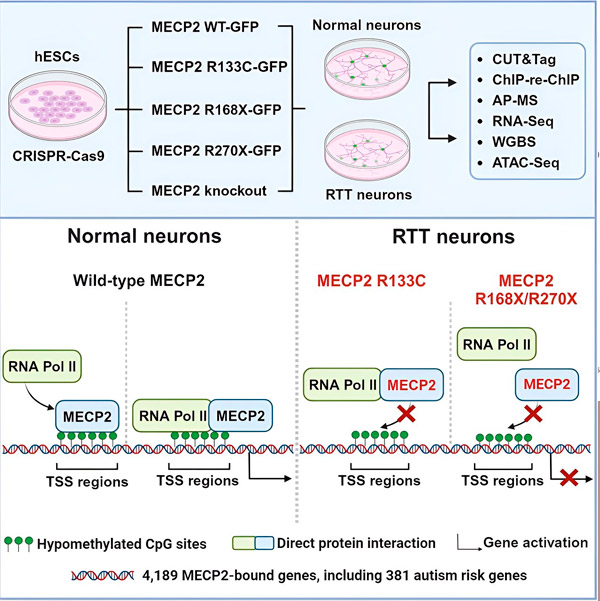
Sursă: Neuron (2024). DOI: 10.1016/j.neuron.2024.04.007
Aceste descoperiri pot ajuta la clarificarea mecanismelor care stau la baza simptomelor autismului în sindromul Rett și pot oferi un bun punct de plecare pentru investigarea posibilului rol al MECP2 în autism.
„Am creat prima hartă integrată a epigenomului MECP2 în sănătate și boală, iar această hartă poate ghida cercetările viitoare”, spune Liu. „Cunoașterea genelor care sunt ținte ale MECP2 și a genelor care sunt perturbate direct în boală oferă o bază solidă pentru înțelegerea sindromului Rett și pentru a pune întrebări despre reglarea genelor în neuroni.”
Cercetătorii au analizat, de asemenea, dacă MECP2 a crescut sau a scăzut expresia genelor sale țintă. În concordanță cu istoricul identificării MECP2 de către unii ca activator și de către alții ca represor, Liu și Flamier au găsit exemple în care MECP2 a jucat ambele roluri.
Totuși, deși MECP2 este mai des considerat un represor, Liu și Flamier au descoperit că este în mare parte un activator – confirmând descoperirile anterioare ale lui Jaenisch și Liu. Un nou experiment a arătat că MECP2 activează cel puțin 80% din țintele sale, iar un altul a constatat că activează până la 88% din țintele sale.
Harta genelor țintă creată de cercetători a oferit informații suplimentare despre rolul MECP2 ca activator. Aceștia au descoperit că, în cazul genelor pe care MECP2 le activează, aceasta se leagă de obicei de o regiune a ADN-ului în amonte de genă, numită situs de inițiere a transcripției.
Acesta este locul în care mecanismele celulare inițiază procesul de transcriere a unei gene în ARN, după care ARN-ul este tradus într-o proteină funcțională, care este produsul expresiei genelor. Prezența MECP2 la locul de începere a transcripției, unde începe expresia genelor, este în concordanță cu rolul său de activator genetic.
Cercetătorii au început apoi să determine ce rol joacă MECP2 în activarea genelor. Au analizat moleculele de care se leagă MECP2 la acest loc, pe lângă ADN, și au descoperit că MECP2 interacționează direct cu un complex proteic numit ARN polimerază II (ARN Pol II). ARN Pol II este o mașinărie celulară cheie care transcrie ADN-ul în ARN. ARN Pol II nu poate găsi gene pe cont propriu, așa că necesită o varietate de cofactori, sau colaboratori proteici, pentru a-și face treaba.
Cercetătorii propun că MECP2 servește drept un astfel de cofactor, ajutând ARN Pol II să inițieze transcripția la genele de care se leagă MECP2. Analiza structurală a MECP2 a identificat părți ale moleculei care se leagă de ARN Pol II, iar alte experimente au confirmat că pierderea MECP2 reduce prezența ARN Pol II la locurile de începere a transcripției adecvate, precum și nivelurile de expresie ale genelor țintă.
Acest lucru sugerează că sindromul Rett ar putea fi cauzat de scăderea transcripției genelor vizate de MECP2, din cauza mutațiilor MECP2 care împiedică legarea acestuia la ARN Pol II sau la ADN. În concordanță cu această idee, cele mai frecvente mutații MECP2 asociate cu boala sunt trunchierile: mutații în care lipsește o parte a proteinei, ceea ce poate altera interacțiunea dintre MECP2 și ARN Pol II.
Cercetătorii speră că descoperirile lor nu numai că vor schimba înțelegerea noastră asupra MECP2, ci și că o înțelegere mai profundă și mai largă a modului în care MECP2 influențează dezvoltarea și funcția creierului ar putea duce la noi perspective care vor ajuta persoanele cu sindrom Rett și tulburări înrudite, inclusiv autism.
„Acest proiect este un exemplu excelent al naturii colaborative a laboratorului Janisch”, spune Flamier. „Eu și Rudolf am avut o problemă specifică legată de sindromul Rett, iar eu aveam experiență cu tehnologia CUT&Tag, care ar putea rezolva problema. Prin discuții, ne-am dat seama că ne putem uni eforturile, iar acum avem o colecție excelentă de informații despre MECP2 și legăturile sale cu bolile.”
