Noile publicații
Derivații compușilor talidomidei conduc la moartea celulelor canceroase rezistente
Ultima examinare: 02.07.2025

Tot conținutul iLive este revizuit din punct de vedere medical sau verificat pentru a vă asigura cât mai multă precizie de fapt.
Avem linii directoare de aprovizionare stricte și legătura numai cu site-uri cu reputație media, instituții de cercetare academică și, ori de câte ori este posibil, studii medicale revizuite de experți. Rețineți că numerele din paranteze ([1], [2], etc.) sunt link-uri clickabile la aceste studii.
Dacă considerați că oricare dintre conținuturile noastre este inexactă, depășită sau îndoielnică, selectați-o și apăsați pe Ctrl + Enter.
Un studiu realizat de Universitatea Goethe din Frankfurt indică posibilitatea ca derivații de talidomidă să poată fi utilizați pentru tratarea cancerului. Talidomida a fost vândută ca somnifer în anii 1950. Ulterior, a devenit cunoscută pentru faptul că provoacă malformații congenitale severe în primele etape ale sarcinii.
Molecula este, de asemenea, cunoscută pentru faptul că marchează proteinele din celulă pentru distrugere. Ca parte a studiului actual, oamenii de știință au creat derivați ai talidomidei. Ei au reușit să demonstreze că aceste substanțe afectează distrugerea proteinelor responsabile de supraviețuirea celulelor canceroase.
Poate că nicio altă moleculă nu a avut un trecut atât de turbulent precum talidomida. A fost ingredientul principal al unui medicament aprobat în multe țări în anii 1950 ca sedativ și somnifer. Dar a devenit curând clar că femeile însărcinate care luau talidomidă nășteau adesea copii cu deformități grave.
Cu toate acestea, în ultimele decenii, medicina și-a pus din nou mari speranțe în el. Studiile au arătat, printre altele, că inhibă creșterea vaselor de sânge și, prin urmare, este potențial potrivit pentru separarea tumorilor din mediul lor nutritiv. Apoi, s-a dovedit a fi foarte eficient și în tratamentul mielomului multiplu, tumori maligne din măduva osoasă.
„Știm acum că talidomida poate fi numită un «adeziv molecular»”, explică Dr. Xinglai Cheng de la Institutul de Chimie Farmaceutică al Universității Goethe din Frankfurt. „Aceasta înseamnă că este capabilă să prindă două proteine și să le unească.”
Acest lucru este deosebit de interesant deoarece una dintre aceste proteine este un fel de „mașină de etichetat”: atașează o etichetă lipsită de ambiguitate „GUNOI” unei alte proteine.
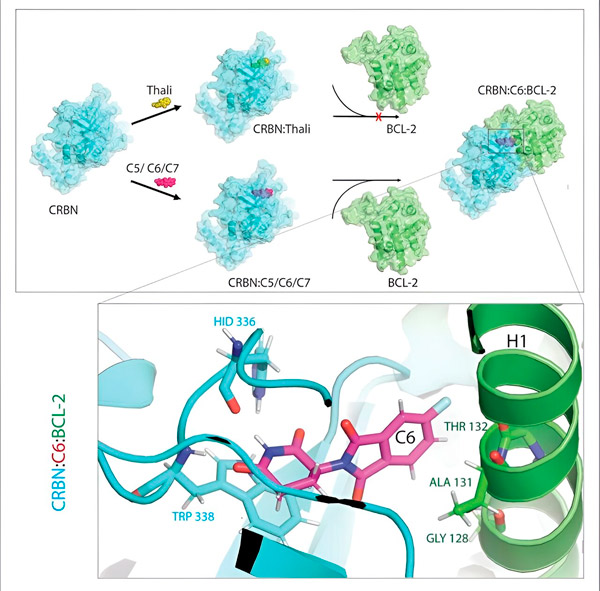
Derivații de talidomidă C5, C6 și C7 modifică CRBN, „mașina de marcare”, astfel încât aceasta se poate lega de BCL-2. În acest fel, molecula BCL-2 este marcată pentru degradare - o posibilă nouă strategie de combatere a cancerului. Autor: Dr. Xinglai Cheng.
Sistemul de eliminare a deșeurilor al celulei recunoaște această etichetă: prinde molecula proteică etichetată și o mărunțește. „Acest mecanism explică diferitele efecte ale talidomidei”, spune Cheng. „În funcție de proteina etichetată, aceasta poate provoca deformări în timpul dezvoltării embrionare sau poate distruge celulele maligne.”
Acest mecanism deschide mari posibilități pentru medicină, deoarece celulele canceroase depind de anumite proteine pentru a supraviețui. Dacă acestea ar putea fi direcționate sistematic și mărunțite, poate că boala ar putea fi vindecată. Problema este că lipiciul molecular este destul de particular.
Unul dintre partenerii săi de legare este întotdeauna mașina de marcare a celulei sau, în limbaj științific, o ligază E3 numită CRBN. Doar foarte puține dintre miile de proteine din organism pot fi al doilea partener - care dintre ele depinde de adeziv.
„Așadar, am creat o serie de derivați de talidomidă”, spune Cheng. „Apoi am testat dacă aveau proprietăți adezive și, dacă da, împotriva căror proteine erau eficienți.” Pentru a face acest lucru, cercetătorii au adăugat derivații lor la toate proteinele din linia celulară cultivată. Apoi au observat care dintre aceste proteine au fost apoi degradate în prezența CRBN.
„În acest proces, am identificat trei derivați care ar putea marca o proteină celulară foarte importantă pentru degradare, BCL-2”, explică Cheng. „BCL-2 împiedică celulele să își activeze programul de autodistrugere, așa că, dacă nu este prezentă, celulele mor.”
De aceea, BCL-2 a fost mult timp un punct central al cercetării în domeniul cancerului. Există chiar și un medicament pentru leucemie numit venetoclax, care reduce eficacitatea BCL-2 și, prin urmare, provoacă autodistrugerea celulelor mutante.
„Totuși, în multe celule canceroase, BCL-2 în sine este mutat. Drept urmare, venetoclaxul nu mai inhibă proteina”, spune Cheng. „Am reușit să demonstrăm că derivații noștri semnalează și această formă mutată pentru degradare. În plus, partenerii noștri de la Institutul Max Planck pentru Biofizică au simulat interacțiunea derivaților de talidomidă cu BCL-2 pe un computer. Acest lucru a arătat că derivații se leagă de situsuri complet diferite față de venetoclax - un rezultat pe care l-am putut confirma ulterior experimental.”
Cercetătorii și-au testat compușii și pe muște de fructe cu celule canceroase. Rata de supraviețuire a muștelor tratate în acest mod a fost semnificativ mai mare. Cu toate acestea, Cheng avertizează împotriva așteptărilor excesive, deoarece aceste rezultate sunt încă cercetări de bază. „Deși arată că moleculele de talidomidă modificate au un mare potențial terapeutic, nu putem spune încă dacă își vor dovedi eficiența în practică la un moment dat.”
Rezultatele studiului au fost publicate în revista Cell Reports Physical Science.
